Un paciente de 20 años, quien había migrado desde Méjico a los EE UU 3 meses antes se presentó al departamento de emergencies, refiriendo que había tenido pérdida de peso y dolor en cadera y region lumbar baja. El paciente no hablaba ingles, por lo que la historia clínica se obtuvo con el uso de el limitado conocimiento de español del equipo medico con la ayuda de improvisados intérpretes no entrenados. Dos semanas antes del comienzo de la enfermedad actual, el paciente se había resbalado y caído en un piso mojado. Aunque no refirió dolor importante en el momento ni inmediatamente después de la caída, varios días después comenzó a sentir dolor en la region lumbar baja derecha y en cadera derecha. El paciente describía dolor de tipo punzante, intermitente, que aumentaba con los movimientos. Notó además pérdida de apetito y descenso no intencional de 16 kg de peso. Refirió cefalea bitemporal, mareos y nauseas así como fatiga fácil con leve dificultad respiratoria (refería “respiración corta”). Dijo no haber tenido fiebre, escalofríos, sudoración nocturna, confusion diarrea, constipación, vómitos, urgencia urinaria tos, ni aparición de púrpura.
El paciente refería que la pérdida de apetito desde que había discontinuado el ácido valproico 3 semanas antes de la presentación. Él había estado tomando dicha medicación desde los 13 años de edad por diagnóstico de gran mal epiléptico. En ese momento el había estado internado en Méjico, donde se le aconsejó que debía tomar la medicación el resto de su vida. El paciente dijo no consumer alcohol, tabaco ni drogas ilícitas. Tenía una compañera sexual estable. Vivía con un primo y trabajaba en un supermercado.
El paciente estaba alerta, pero impresionaba caquéctico. Su altura era de 1,65 mts y su peso 47 kg. La temperatura oral era de 37,3°C, la TA 95/63 mmHg, y su pulso 93 por minuto. El examen cardiopulmonar no revelaba anormalidades. Tenía una esplenomegalia palpable y una hepatomegalia medida de 12 cm, pero no se quejaba de dolor abdominal. Tenía leve dolor a la percussion de la region lumbar derecha baja así como a la rotación externa pasiva de la cadera derecha. Un examen neurológico reveló una marcha lenta e insegura, debilidad generalizada, sin déficits focales y reflejos simétricos y normales. La maniobra de Romberg fue negativa y no había temblor ni dismetría. No había rash, petequias, linfadenopatías, ni ictericia conjuntival. El examen del fondo de ojo y genitourinario no fueron llevados a cabo. El resto del examen físico era negativo.
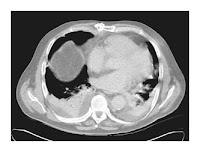
El recuento de blancos era de 4000/mm3 con 52% de polimorfonucleares, 4% en cayado, 4% de monocitos, 39% de linfocitos y 1% de metamielocitos. Su nivel de hemoglobina era de 13,8 g/dl, con evicencias de teardrop (células en lágrima), acantocitos, poiquilocitos y ovalocitos en el frotis de sangre periférica. Las plaquetas eran de 20000/mm3. El resultado de análisis completos de laboratorio químico fue normal excepto por la FAL 199 U (normal 40 a 120 U/L) TGO 147 (16 a50) TGP 75 (12 a 61) y LDH 1115 U(normal 313 a 618). Los estudios de coagulación fueron normales. El nivel de amilasa fue 136 U/L (normal 30 a 110/L), lipase 419 U/L (normal 23 a 300). Los niveles de ácido valproico fueron indetectables, y el resultado de los tests toxicológicos fueron negativos. La eritrosedimentación era normal de 4 mm/hora. La PCR de 3,1 mg% (normal menos de 0,8). Las Rx de tórax, caderas y columna lumbosacra fueron normales. Una TAC de craneo mostró una lesion calcificada de 2 mm de largo en el lóbulo frontal. Una TAC de abdomen y pelvis mostró edema difuso hepático y esplenomegalia. Los cultivos de sangre y orina fueron negativos.
El paciente fue tratado con ibuprofeno y acetaminophen por el dolor. En el hospital notó fiebre nocturna de 38,5°C a 40°C. El 2° día de hospital, un soplo cardiaco Nuevo fue auscultado, y el paciente comenzó a referir dolor en el codo izquierdo, similar al de la cadera derecha. Los hemocultivos tomados a su ingreso no presentaban crecimiento de microorganismos. El HIV fue negative. Un test cutaneo de tuberculina fue negative, pero el test con cándida y parotiditis también fueron negativos evidenciando anergia. El monotest para mononucleosis, hepatitis A, B yC fueron todos negativos.
Una PAMO mostró una médula normocelular con leve hyperplasia mieloide , disminución de los depósitos de hierro y escasos granulomas no caseosos (Figura 1). Una tinción de médula fue negativa para bacilos ácido alcohol resistentes. Un centelleograma obtenido con el uso de difosfonato marcado con tecnecio 99 reveló leve captación asimétrica en el tobillo derecho y sacroilíaca derecha que fue interpretado como cambios degenerativos; sin embargo no se pudo descartar osteomielitis. Un ecocardiograma transtorácico y transesofágico no mostraron evidencias de vegetaciones, y la function cardiaca estaba normal.
, disminución de los depósitos de hierro y escasos granulomas no caseosos (Figura 1). Una tinción de médula fue negativa para bacilos ácido alcohol resistentes. Un centelleograma obtenido con el uso de difosfonato marcado con tecnecio 99 reveló leve captación asimétrica en el tobillo derecho y sacroilíaca derecha que fue interpretado como cambios degenerativos; sin embargo no se pudo descartar osteomielitis. Un ecocardiograma transtorácico y transesofágico no mostraron evidencias de vegetaciones, y la function cardiaca estaba normal.
Cual es el diagnóstico?En el 7° día de hospital un test serológico para brucella fue positivo con un título mayor de 1/160. Al siguiente día los cultivos repetidos de sangre y médula ósea fueron positivos para cocobacilos gram(-), subsecuentemente identificados como Brucella abortus. El paciente fue tratado con doxiciclina y rifampicina. Estuvo afebril, el soplo desapareció y el dolor de la cadera, lumbalgia y codo desaparecieron en pocos días. Durante la hospitalización, detalles adicionales de la historia clínica fueron obtenidos con la ayuda de un intérprete. El paciente había trabajado durante 3 años en un matadero y refirió contacto con ganado vacuno, ovino y porcino faenados.
Comentario:
La brucelosis es una enfermedad zoonótica que puede afectar cualquier sistema orgánico. La mayoría de los casos en el humano son causados por contacto con animales o sus productos tales como leche no pasteurizados y queso. Cuatro especies son responsables de los casos humanos: B abortus (encontrada en Ganado vacuno), B melitensis ( cabras y ovejas), B suis (cerdos), y B canis (perros). La presentación clínica puede ser aguda o progresiva, usualmente comenzando con síntomas inespecíficos tales como fiebre, sudoración, pérdida de peso, artralgias y mialgias.
Tanto la serología como los cultivos son útiles para el diagnóstico. El período de incubación es entre 7 días y 3 meses aunque han sido reportados períodos de incubación de 10 meses!!! Una historia exhustiva sobre viajes así como historia de exposición a animales y alimentos es crítica al momento de formular el diagnóstico presuntivo.
Retrospectivamente, este paciente tuvo síntomas clásicos de brucelosis; sin embargo tomó varios días antes de que el grupo médico asistente hiciera el diagnóstico correcto. La presentación inicial fue compatible con otras enfermedades consideradas mas comunes, que incluian tuberculosis, endocarditis, infecciones fúngicas, cánceres hematológicos, y enfermedades relacionadas con HIV y a descartar o confirmar las mismas se dirigieron los esfuerzos iniciales. En un momento de la evolución se consideró correctamente la posibilidad de tuberculosis aún con test cutáneos negativos, ya que la presencia de la misma sin tratamiento podría evolucionar fatalmente sin tratamiento.
Después de la internación el paciente notó fiebre alta durante la noche. Los médicos tratantes decidieron reclasificar el cuadro como fiebre de origen desconocido, aunque aún no cumplía 3 semanas de fiebre. Una parte crítica de la evaluación también incluye una historia clínica completa, que inicialmente estuvo comprometida por la barrera del lenguaje. Afortunadamente el uso de intérpretes profesionales permitió eventualmente a los clínicos descubrir información crucial, la exposición ocupacional del paciente, alertando a los médicos a la posibilidad de contacto con brucella. Después de conocerse esta historia de exposición, fueron obtenidos estudios serológicos para brucelosis y los cultivos fueron especialmente monitoreados para desarrollo del germen todo lo cual condujo al diagnóstico definitivo.
Este caso demuestra la importancia de una buena comunicación dialéctica médico paciente y la necesidad de que la comprensión entre ambos culmine con un correcto diagnóstico. Fue necesaria la intervención de un intérprete , a la vez médico para obtener información que finalmente fue crítica en el desenlace del caso.
Por ahora, nuestro país no tiene niveles masivos de inmigración como los EEUU donde esta historia se desarrolló, pero hay que considerar que los resultados de la globalización, especialmente en los grandes centros urbanos nos van a exponer cada vez mas a las barreras linguísticas para lo que debemos estar preparados.
From the Department of Medicine, University of Utah, Salt Lake City the Department of Veterans Affairs
 Nefrocalcinosis:
Nefrocalcinosis: