|
| Hospital Municipal "Dr Ángel Pintos" |
Mujer de 32 años
MOTIVO DE INTERNACIÓN: extrasistolia ventricular con criterios
de malignidad
ENFERMEDAD ACTUAL: es traída a la guardia del
hospital por servicio de emergencia por haberse despertado con “sensación de
muerte”, malestar general, mareos. Inicialmente interpretada como “crisis
nerviosa” se aplicó diacepan 10mg IM y se realiza ECG que muestra aritmia
compleja por extrasístoles ventriculares frecuentes que ceden espontáneamente
al igual que todo el cuadro.
ANTECEDENTES DE ENFERMEDAD ACTUAL: antecedentes de episodios de nerviosismo, episodios
fugaces de palpitaciones. Diarrea que atibuye a “estados nerviosos”.Quince días
antes de la internación actual consultó a su médico por palpitaciones por lo
que se reduce la dosis de T4 que toma desde hace varios años. Posteriormente
se reciben dosajes de hormonas tiroideas solicitados al momento de dicha consulta (antes de modificar la dosis): TSH 0,41mU/L (normal 0,4 a 4,5). T4 libre 2,2ng/dl (normal 0,7 a 1,8).
Dos días antes de esta internación recibió
analgésicos por contractura cérvico-dorsal. Refiere asimismo en los últimos 7
días calambres en gemelos.
ANTECEDENTES PERSONALES Y PATOLÓGICOS: Hipotiroidismo desde hace 13 años. HTA diagnosticada hace 1 año. Le explicaron que la misma se relacionaba con su "personalidad nerviosa". "Extrasistolia", refiere que le han diagnosticado extrasístoles en varias consultas y algunos electrcardiogramas pero que siempre le dijeron que eran "benignas" y que no requerían estudio ni tratamiento específico. Según le dijo su madre tuvo sufrimiento fetal al final de su gesta.
Fecha de última menstruación 1 mes antes. Eva test
actual (-) Tomó anticonceptivos hasta hace 1 mes
ANTECEDENTES FAMILIARES: Madre arritmia. Padre: ACV, DBT2, HTA, Dislipemia
Abuelo fallecido de muerte súbita a los 50 años
HÁBITOS: alcohol escaso los fines de semana, tabaco
no. Dieta general. Medicación actual
valsartan 80 mg atenolol 50 mg y 25 mg de hidroclorotiazida/día, levotiroxina
125 ug/día
Trabaja como empleada en un comercio
EXAMEN FÍSICO: lúcida, TA 170/100 mm Hg frecuencia
65 por minuto. Temperatura 36,2°C
Frecuencia respiratoria 20 por minuto. Saturación de
O2 98% respirando aire ambiente.
Tórax y abdomen s/p
Se solicitan análisis de rutina y de los cuales
llama la atención Hipopotasemia severa 1,1 meq/l, Na 147, creatinina 2 mg/dl. y CPK
7905 UI/L
Ionograma en orina: Na: 54,2 K: 27,25, Cl: 61,1. Volumen diurético
2600 ml/24 hs
Se indica potasio EV, Mg y K por vía oral.
Interconsulta con cardiología: Paciente con HTA
tratada crónicamente con valsartán, diuréticos y betabloqueantes que ingresa por arritmia
ventricular asociada a QT largo, HVI. Se objetiva hipopotasemia severa.
Pendiente eco 2D. Se interpreta como hipopotasemia asociada a diuréticos.
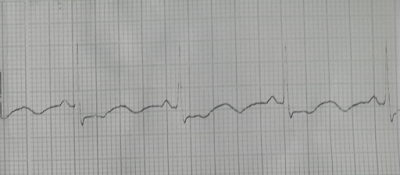
Informe del ECG:
Ritmo sinusal. FC 71 Eje eléctrico de QRS 0* Onda P.
QTc 566 mes PR 140 mseg QRS 90 mseg. Infradesnivel
horizontal del ST en dos derivaciones que creo son DI, DII, AVF. Sin embargo no
tanto en DIII ni en AVL. Pero sí es infradesnivel de 2 mm y horizontal que
traduce lesión subendocardica. Arritmia ventricular extra sistolica con
tripletas, dupletas polimorficas. Ecocardiograma y eco Doppler no muestran HVI,
FS conservada, pericardio libre, resto s/p. Se solicitó ecografía abdominal y
TC para evaluar suprarrenales.
 |
D1
|
 |
D2
|
 |
D3
|
 |
| aVR |
 |
| aVL aVF |
 |
V1 V2 V3
|
 |
| V4 |
 |
| V5 V6 |
 |
| RITMO |
Ecocardiograma y eco Doppler no muestran HVI, FS
conservada, pericardio libre, resto s/p.
Se solicitó ecografía abdominal y TC para evaluar
suprarrenales.
Tomografía computada de abdomen: litiasis vesicular. Se observa imagen
hipodensa de 27 X 17 mm en suprarrenal
derecha que realza con la administración de contraste EV compatible con
adenoma.
 |
| La flecha marca el adenoma adrenal derecho |
 |
| Añadir leyenda |
Después de tomar muestras de sangre para
aldosterona, renina, cortisol plasmático, CLU, ácido vanil mandélico y
catecolaminas plasmáticas se comenza con espironolactona 200 mg/día, potasio
por VO, y eventual enalapril si la TA es mayor a 140/90 mm Hg.
Se reciben los valores de laboratorio hormonales:
Actividad de renina plasmática: menos de 0,6 ng/mL/hora.
Aldosterona plasmática: 30 ng/dl
Relación Aldosterona/renina 50.
Valores de CLU, vanilmandélico y catecolaminas
plasmáticas y urinarias dentro de los valores normales
Se interpreta el cuadro como hiperaldosteronismo primario secundario a adenoma suprarrenal
derecho funcionante. Se consideró innecesario el dosaje diferencial de aldosterona en ambas venas suprarrenales para confirmar lateralización y se indicó cirugía laparoscópica de la glándula adrenal derecha a lo que la paciente y su esposo se opusieron. A la paciente se le ofreció continuar con tratamiento médico con espironolactona 100mg cada 12 horas y controles clínicos e imagenológicos por consultorio externo.
Seis meses y un año después del diagnóstico, la paciente se encuentra asintomática, su TA es de 128/86 mmHg,supotasio plasmático es de 4,1 meq/L y el tamaño del adenoma no se ha modificado.
HIPERALDOSTERONISMO PRIMARIO (SÍNTESIS)
Aunque inicialmente se consideró una rareza, el
aldosteronismo primario ahora se considera una de las causas más comunes de
hipertensión secundaria ( HTA ). Litynski informó los primeros casos, pero Conn
fue el primero en caracterizar bien el trastorno en 1956. El síndrome de Conn,
como se describió originalmente, se refiere específicamente al aldosteronismo
primario debido a la presencia de un aldosteronoma suprarrenal (neoplasia
suprarrenal benigna secretora de aldosterona).
Con base en datos más antiguos, originalmente se
estimó que el aldosteronismo primario representaba menos del 1% de todos los
pacientes con HTA. Datos posteriores, sin embargo, indicaron que en realidad
puede ocurrir hasta en un 5-15% de los pacientes con HTA. Aldosteronismo
primario puede ocurrir en un porcentaje aún mayor de pacientes con HTA
resistente al tratamiento y puede estar considerablemente infradiagnosticado;
esto es especialmente cierto si los pacientes con HTA refractaria al
tratamiento no son remitidos específicamente para su evaluación a un endocrinólogo.
Aunque el aldosteronismo primario sigue siendo un
desafío diagnóstico considerable, el reconocimiento de la enfermedad es crítico
porque la HTA asociada al aldosteronismo primario a menudo se puede curar (o al
menos controlar de forma óptima) con la intervención quirúrgica o médica
adecuada. El diagnóstico generalmente es de 3 niveles, lo que implica un
cribado inicial, una confirmación del diagnóstico y una determinación del
subtipo específico de aldosteronismo primario.
Aunque estudios previos sugirieron que los
aldosteronomas eran la causa más común de aldosteronismo primario (70-80% de
los casos), el trabajo epidemiológico posterior indicó que la prevalencia de
aldosteronismo debido a hiperplasia suprarrenal idiopática bilateral (HIB), es
mayor de lo que había sido creído previamente. Estos informes sugieren que la
HIB puede ser responsable de hasta el 75% de los casos de aldosteronismo
primario. Además, los informes han descrito un raro síndrome de aldosteronismo
primario caracterizado por características histológicas intermedias entre el
adenoma suprarrenal y la hiperplasia suprarrenal, que a menudo se localiza
unilateralmente (también se refirió a la literatura anterior como
"aldosteronismo intermedio") .
Figura 1. Imagen de resonancia magnética (MRI) en un
paciente con síndrome de Conn que muestra un adenoma suprarrenal izquierdo.
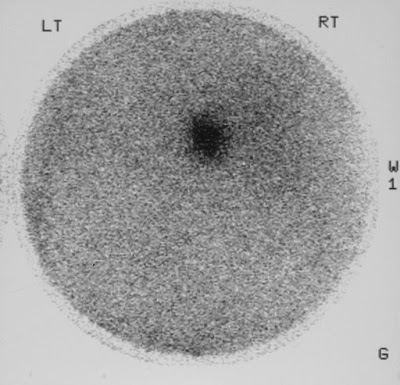
Figura 2. El escintigrama obtenido mediante el uso
de yodo-131-beta-yodometil-norcolesterol (NP-59) en un hombre de 59 años con
hipertensión muestra una captación de radionúclidos bastante intensa en el
tumor adrenal derecho. En la cirugía, se confirmó un tumor de Conn.
Clínicamente, la distinción entre las 2 principales
causas del aldosteronismo primario es vital porque el tratamiento de elección
para cada uno es marcadamente diferente. Si bien el tratamiento de elección
para los aldosteronomas es la extirpación quirúrgica, el tratamiento de
elección para la HIB es el tratamiento médico con antagonistas de la
aldosterona.
Las entidades que se sabe que causan aldosteronismo
incluyen lo siguiente:
- Adenomas productores de aldosterona (APA) [ 1 ]
- Adenomas productores de aldosterona sensible a la
renina (AP-RAs, también abreviado como RRAs)
- Hiperplasia suprarrenal idiopática bilateral
(glomerulosa) o HIB (también conocida como hiperplasia suprarrenal primaria o
HSP)
- Formas familiares de aldosteronismo primario
- Secreción ectópica de aldosterona (los ovarios y
los riñones son los dos órganos descritos en la literatura que, en el contexto
de una enfermedad neoplásica, que pueden ser fuentes ectópicas de aldosterona,
pero esto es raro).
- Carcinomas suprarrenales productores de
aldosterona puros (muy raros; fisiológicamente se comportan como APA)
La aldosterona, al inducir la reabsorción renal de
sodio en el túbulo contorneado distal (TCD), aumenta la secreción de iones de
potasio y de hidrógeno, causando hipernatremia, hipocalemia y alcalosis.
ALDOSTERONISMO PRIMARIO GENÉTICO-FAMILIAR
Existen tres variedades genético-familiares
distintas de aldosteronismo primario. Sutherland y sus colegas describieron por
primera vez la variedad tipo 1 de aldosteronismo primario familiar,
aldosteronismo remediable con glucocorticoides (GRA), en 1966. En GRA, la HTA
responde clínicamente a pequeñas dosis de glucocorticoides además de otros
agentes antihipertensivos. [ 2 ]La forma tipo 1 de aldosteronismo primario
familiar se debe a un producto génico quimérico aberrante formado que combina
el promotor sensible a glucocorticoides (inhibidor) del gen de la
11beta-hidroxilasa (CYP11B1) con la región codificante del gen de la
aldosterona sintetasa (CYP11B2). En niveles de glucocorticoides ambientales, el
promotor no se silencia por completo de la transcripción, y esto conduce a la
sobreexpresión de la aldosterona sintetasa, con el consiguiente aumento de la
síntesis y secreción de aldosterona.
La variante tipo 2 del aldosteronismo primario
familiar (que no es sensible a los glucocorticoides) se describió por primera
vez en 1991. Aunque no se ha identificado la anomalía genética exacta para el
aldosteronismo primario tipo 2, los datos sugieren que el locus para esta
enfermedad está en la banda 7p22. [ 3 ]
La variante tipo 3 del aldosteronismo primario
familiar se debe a KCNJ5 (canal de rectificación interior del potasio,
subfamilia J, miembro 5) mutaciones del canal de potasio. Este tipo fue
descrito por el grupo Lifton en 2011. [ 4 ]
DIAGNÓSTICO
1 PRUEBAS DE DETECCIÓN (DE PRIMER NIVEL) PARA EL
ALDOSTERONISMO PRIMARIO INCLUYEN LAS SIGUIENTES:
ANiveles séricos de potasio y bicarbonato
B Niveles de sodio y magnesio
C Relación de actividad plasmática de aldosterona /
renina plasmática
2 LAS PRUEBAS DE CONFIRMACIÓN (SEGUNDO NIVEL)
INCLUYEN LO SIGUIENTE:
A Nivel de aldosterona sérica
B Prueba de excreción de aldosterona en orina de 24
horas
C Prueba de carga de sal
3 PRUEBAS PARA DETERMINAR EL SUBTIPO DE
ALDOSTERONISMO PRIMARIO (PRUEBAS DE TERCER NIVEL) INCLUYEN LAS SIGUIENTES:
A Prueba de estimulación postural
B Prueba de estimulación de furosemida (Lasix)
C Ritmo diurno de la aldosterona
LA INVESTIGACIÓN RADIOLÓGICA INICIAL EN EL ESTUDIO
DEL ALDOSTERONISMO PRIMARIO ES LA TOMOGRAFÍA COMPUTARIZADA (TC) SUPRARRENAL DE ALTA RESOLUCIÓN Y CORTE FINO (2-2,5 mm) CON CONTRASTE.
Otras pruebas incluyen lo siguiente:
CENTELLOGRAFÍA CON YODO-METIL-NORCOLESTEROL NP-59:
aunque es bastante difícil de establecer y no está disponible de forma
rutinaria, esta prueba puede ser útil en casos seleccionados para distinguir
entre adenomas e hiperplasia.
MUESTREO VENOSO SUPRARRENAL: el muestreo venoso
suprarrenal probablemente tiene su mayor utilidad cuando los hallazgos de
imágenes suprarrenales son completamente normales a pesar de la evidencia
bioquímica de aldosteronismo primario y en escenarios en los que la patología
suprarrenal bilateral está presente en imágenes y la bioquímica sugiere la
presencia de un aldosteronoma funcional
PRUEBA DE SUPRESIÓN DE DEXAMETASONA: esta prueba es
relevante solo en el contexto de un posible aldosteronismo familiar
PRUEBA DE METOCLOPRAMIDA (REGLAN): esta es una
prueba no invasiva para distinguir entre aldosteronomas e hiperplasia
suprarrenal idiopática (HSI)
MANEJO
La terapia farmacológica incluye el uso de lo
siguiente:
- Bloqueadores de los canales de calcio
- Antagonistas de mineralocorticoides
- Glucocorticoides
La cirugía es el tratamiento de elección para las
variantes lateralizables del aldosteronismo primario, incluidos los
aldosteronomas típicos, los adenomas sensibles a la renina (RRA) y la
hiperplasia suprarrenal primaria (HAP). Una adrenalectomía se puede realizar a
través de una laparotomía formal o mediante el uso de una técnica laparoscópica
(con la utilización de este último método cada vez más común).
FISIOPATOLOGÍA
- Los factores más importantes que aseguran la
hipocalemia en el aldosteronismo
primario son: hipersecreción de aldosterona, que actúa sobre el conducto
colector cortical para estimular la secreción de potasio en el líquido tubular,
aumentando así la pérdida renal /
urinaria de potasio [ 5 ] ;
- Volumen intravascular adecuado, que permite un
suministro adecuado de agua (flujo
tubular) a los túbulos contorneados distales (TCD) y los conductos colectores
para permitir la pérdida renal de potasio;
- Ingesta adecuada de sodio en
la dieta, lo que a su vez aumenta el potasio corporal total, el suministro
renal / tubular de sodio y, por lo tanto, aumenta la pérdida renal de potasio a
través del sistema de transporte en contracorriente.
La ausencia de una o más de las circunstancias
fisiológicas descritas anteriormente puede explicar la ausencia de hipocalemia
franca en muchos pacientes con aldosteronismo primario comprobado.
La alcalosis metabólica asociada en el
aldosteronismo primario se debe a una mayor pérdida renal de iones de hidrógeno
mediada por hipocalemia y aldosterona.
Casi el 20% de los pacientes con aldosteronismo
primario tienen intolerancia a la glucosa como resultado del efecto inhibidor
de la hipocalemia sobre la acción y secreción de la insulina; sin embargo, la
diabetes mellitus no es más común que en la población general.
ETIOLOGÍA
La anomalía cardinal que causa el síndrome de
aldosteronismo primario es la producción de aldosterona autónoma (no
suprimible). Además de la producción de aldosterona no suprimible, los niveles
de renina plasmática suprimidos
coexisten conun volumen volumen
de líquido intratravascular y extravascular muy levemente expandido. La
regulación normal de la secreción de aldosterona está mediada en diversos
grados por la renina, los niveles séricos de potasio y sodio, el estado del
volumen intravascular y la corticotropina.
La regulación de la producción de aldosterona por
estos factores puede alterarse de diversas maneras, según el subtipo de
aldosteronismo primario. Generalmente, los adenomas productores de aldosterona
(APA) y GRA siguen siendo sensibles a la corticotropina, mientras que la
hiperplasia suprarrenal idiopática (IAH) y los adenomas sensibles a la renina
(RRA) productores de aldosterona mantienen la respuesta al sistema
renina-angiotensina (RAS).
En aldosteronismo remediable con glucocorticoides
(GRA), se suprime el RAS y la aldosterona se regula mediante corticotropina
debido a la fusión del gen quimérico de un promotor sensible a la
corticotropina con las regiones codificantes del gen de la aldosterona
sintetasa (que normalmente no tiene dicho promotor ) Por lo tanto, los niveles
de corticotropina ambiental patológicamente sobreestimulan la síntesis de
aldosterona inapropiadamente. [ 6 ]
En pacientes con aldosteronismo remediable con glucocorticoides
(GRA), la administración de dexametasona (o cualquier otro glucocorticoide) a
dosis suficientes para suprimir la producción excesiva de corticotropina da
como resultado una reducción en la síntesis de aldosterona y natriuresis y la
eventual corrección de las anomalías bioquímicas del aldosteronismo primario. [
7 ] Los estudios histológicos en esta enfermedad han mostrado hiperplasia
específica de la zona fasciculada, con atrofia concomitante de la zona
glomerular.
CAUSAS
La causa exacta del aldosteronismo primario
esporádico debido a un adenoma o hiperplasia no está clara. La existencia de
factores tróficos (p. Ej., Endotelinas, citocinas) se ha postulado en casos de
hiperplasia. Las mutaciones somáticas de los genes que conducen a una ventaja
de crecimiento en el tejido adenomatoso suprarrenal son una causa posible, pero
no probada.
En formas familiares de aldosteronismo primario, se
conoce la base molecular de GRA. GRA se debe a una mutación que resulta de un
producto genético híbrido. [ 3 ] Los genes de la 11beta-hidroxilasa y la
aldosterona sintetasa que normalmente se encuentran cerca uno del otro en el
cromosoma 8 se cruzan para crear un nuevo producto genético híbrido. Este gen
híbrido consiste en la secuencia reguladora sensible a la corticotropina del
gen de 11beta-hidroxilasa (CYP11B1) fusionado al componente estructural del gen
de la aldosterona sintetasa (CYP11B2). [ 2 ]
La mayoría de los aldosteronomas esporádicos surgen
de la zona fasciculada, y a menudo tienen una hiperplasia glandular cercana al
adenoma. Esto sugiere que se produce una respuesta proliferativa de las células
a algún factor paracrino / autocrino actualmente no identificado. Dentro de
esta zona de hiperplasia, se cree que tiene lugar un cambio clonal en una sola
célula, proporcionando así el nido para el adenoma en desarrollo.
La base genética del aldosteronismo familiar tipo 2
no está clara; sin embargo, el locus para esta enfermedad se ha mapeado en 7p22
(banda 11q13). [ 3 ] Este síndrome puede manifestarse histológicamente como
hiperplasia o adenomas.
La base genética para el aldosteronismo familiar
tipo 3 se ha descifrado recientemente. Las mutaciones en el gen codificador del
canal de potasio KCNJ5 dan como resultado la pérdida de selectividad iónica, la
despolarización de la membrana celular, el aumento de la entrada de Ca2 + en
las células adrenales de la glomerulosa y el aumento de la síntesis de
aldosterona. [ 4 ]
ALDOSTERONISMO TERCIARIO
La existencia de aldosteronismo terciario como una
entidad separada sigue siendo controvertida. Se presume que la entidad es el
resultado de elevaciones crónicas de los niveles de renina en plasma y
aldosteronismo secundario, lo que finalmente establece un estado de
aldosteronismo no regulado y autónomo con una imagen histológica de hiperplasia
mixta y adenomas en el tejido adrenocortical afectado. Se considera que este
cuadro clinicopatológico es el resultado final irreversible de los efectos
neurohumorales prolongados sobre la resistencia vascular y la hipertrofia
"terminal" del tejido adrenocortical productor de aldosterona.
Existen pocos casos bien descritos, pero en la
mayoría, las glándulas suprarrenales son hiperplásicas, a menudo con
hiperplasia nodular (que puede causar confusión diagnóstica). Prácticamente
todos los casos descritos se encuentran en el contexto de la estenosis de la
arteria renal, lo que complica aún más la atribución del estado hipertensivo al
exceso crónico de aldosterona "inapropiada".
Inicialmente, los niveles de renina son elevados, lo
que es típico del aldosteronismo secundario. Cuando se desarrolla la fase
terciaria (autónoma), el perfil bioquímico cambia a un estado de renina baja /
alta aldosterona. El paradigma es análogo a la patogénesis del
hiperparatiroidismo terciario.
EPIDEMIOLOGÍA
PREVALENCIA EN LOS ESTADOS UNIDOS
La prevalencia exacta del aldosteronismo primario no
está clara, pero las estimaciones sugieren que el 5-15% de los casos de
hipertensión esencial (HTA) pueden deberse al aldosteronismo primario. La
prevalencia de aldosteronismo primario es probablemente más alta en pacientes
que tienen un nivel de potasio sérico bajo, en pacientes que son ancianos y en
pacientes que tienen HTA que es resistente al uso de medicamentos únicos.
PREVALENCIA INTERNACIONAL
No hay evidencia que demuestre que el aldosteronismo
primario, en sus formas más comunes, ocurra en exceso relativo en cualquier
parte del mundo. [ 8 ]
DATOS DEMOGRÁFICOS RELACIONADOS CON LA RAZA, EL SEXO
Y LA EDAD
El aldosteronismo primario ocurre en todo el mundo.
Varios informes sugieren una mayor prevalencia entre los afroamericanos, las
personas de origen africano y, potencialmente, otros negros. Esto parece ser
particularmente cierto de la variante idiopática de hiperplasia suprarrenal
(IAH) de la enfermedad.
Los adenomas productores de aldosterona (APA) son
más comunes en mujeres que en hombres, con una relación de mujer a hombre de 2:
1. El paciente típico con APA es una mujer de entre 30 y 50 años.
PRONÓSTICO
La morbilidad y la mortalidad asociadas con el
aldosteronismo primario, especialmente el síndrome de Conn, se relacionan
principalmente con la hipocalemia y la hipertensión (HTA). [ 9 , 10 ] La
hipocalemia, especialmente si es grave, causa arritmias cardíacas, que pueden
ser fatales.
Las complicaciones de la HTA crónica incluyen
infarto de miocardio, enfermedad cerebrovascular e insuficiencia cardíaca
congestiva. El tratamiento también puede conducir a complicaciones, como
reacciones a los medicamentos y complicaciones de la cirugía.
Existe evidencia de que el aldosteronismo crónico en
sí mismo, en ausencia de presión arterial elevada (p. Ej., Como ocurre en el
aldosteronismo secundario), también se asocia con un mayor riesgo de lesión
cardíaca, que incluye lesión isquémica, hipertrófica y fibrótica. Además, los
estudios han demostrado que los pacientes con aldosteronismo primario son más
propensos a tener o desarrollar hipertrofia ventricular izquierda, accidente
cerebrovascular y síndromes coronarios agudos que los pacientes con grados
similares de HTA por otras causas. [ 11 ] Por supuesto, los pacientes con HTA
por aldosteronismo primario también corren el riesgo de desarrollar todo el
espectro de complicaciones de la HTA crónica, incluida la nefropatía
hipertensiva y la retinopatía.
HISTORIA
La presentación clínica del aldosteronismo primario
no es distintiva, y el diagnóstico correcto requiere un alto índice de sospecha
por parte del médico. Los escenarios clínicos comunes en los que se debe
considerar la posibilidad de aldosteronismo primario incluyen los siguientes:
Pacientes con hipocalemia espontánea o no provocada,
especialmente si el paciente también es hipertenso [ 12 ]
Pacientes que desarrollan hipocalemia severa y / o
persistente en el contexto de dosis bajas a moderadas de diuréticos que
deplecionan de potasio
Pacientes con hipertensión resistente al tratamiento
(HTA refractaria)
Los pacientes con hipocalemia severa reportan
fatiga, debilidad muscular, calambres, dolores de cabeza y palpitaciones.
También pueden tener polidipsia y poliuria por diabetes insípida nefrogénica
inducida por hipocalemia. La HTA de larga duración puede provocar problemas
cardíacos, retinianos, renales y neurológicos, con todos los síntomas y signos
asociados.
En un estudio que comparó los efectos cardíacos del
aldosteronismo primario versus secundario, Cesari et al determinaron que si
bien ambos tipos de aldosteronismo se caracterizaban con frecuencia por
hipertrofia ventricular izquierda y disfunción diastólica, solo el
aldosteronismo primario se asoció con una evidente disfunción sistólica
subclínica. Además, los pacientes con aldosteronismo primario tuvieron
frecuencias cardíacas más bajas y valores de resistencia arterial y resistencia
vascular más altos que aquellos con la condición secundaria, mientras que la
actividad de la renina plasmática fue menor en el aldosteronismo primario que
en el secundario (0,56 frente a 15,00 ng / ml / h, respectivamente). . [ 13 ]
ALDOSTERONISMO PRIMARIO FAMILIAR
Las dos principales variedades familiares de
aldosteronismo primario son el aldosteronismo remediable por glucocorticoides
(GRA, aldosteronismo primario familiar tipo 1) y un tipo no remediable por
glucocorticoides (aldosteronismo primario familiar tipo 2).
El reconocimiento de GRA es particularmente
importante debido a sus implicaciones para los pacientes que son hipertensos y
cuyos miembros de la familia aparentemente no se ven afectados. La HTA,
derrames cerebrales y otros eventos cardiovasculares significativos se
describen en personas jóvenes con este síndrome.
Aunque el síndrome es poco común, los niveles
elevados de sospecha son esenciales para el diagnóstico. Menos de 200 casos
bien validados existen en la literatura. Todos los pacientes con GRA deben ser
tratados médicamente con glucocorticoides y sin cirugía.
Aunque poco común, GRA puede ser más frecuente de lo
que se suponía previamente. Un subgrupo significativo de pacientes con la
variedad normopotasémica más leve de este síndrome probablemente se presume incorrectamente
que tiene una HTA esencial. [ 9 ]
Los antecedentes familiares de HTA (particularmente
con una edad temprana de inicio), HTA en niños, HTA de baja renina y presunta
HIA son las situaciones típicas en las que se debe considerar este diagnóstico.
El tercer tipo de PA familiar, debido a mutaciones
en el gen codificador del canal de potasio KCNJ5, se considera extremadamente
raro, pero también puede conducir a HTA e hipocalemia a una edad muy temprana.
EXAMEN FÍSICO
Los pacientes con aldosteronismo primario no
presentan hallazgos clínicos distintivos, y un alto índice de sospecha basado
en la historia del paciente es vital para realizar el diagnóstico. Los
hallazgos podrían incluir lo siguiente:
Hipertensión (HTA) - Esta condición casi
invariablemente ocurre, aunque se han descrito en la literatura algunos casos
raros de aldosteronismo primario no asociado con HTA.
Debilidad
Distensión abdominal
Íleo por hipokalemia
Hallazgos relacionados con complicaciones de la HTA:
insuficiencia cardíaca, hemiparesia debida a accidente cerebrovascular, soplos
carotídeos, soplos abdominales, proteinuria, insuficiencia renal, encefalopatía
hipertensiva (confusión, cefalea, convulsiones, cambios en el nivel de
conciencia) y cambios retinianos hipertensivos
Es importante tener en cuenta que el aldosteronismo
primario en sí mismo por lo general no se asocia con edema, a pesar del estado
de volumen expandido asociado con este. La falta de edema es el resultado de
natriuresis espontánea y diuresis (llamado "escape de aldosterona")
que ocurre en pacientes con aldosteronismo primario y que parece estar mediado
por el péptido natriurético auricular (ANP). [ 14 , 15 ] Cabe señalar que este
efecto probablemente se basa en la activación del sistema apical ATP / UTP /
P2Y2 (en el nivel del túbulo de conexión / conducto colector), lo que conduce a
una mayor presentación de sodio, que a su vez induce cierre del canal de sodio
epitelial (ENaC), con la disminución resultante en la reabsorción de sodio (es
decir, natriuresis potenciada). [ 16] Por lo tanto, el hallazgo de edema
importante en los pacientes que se presume que tienen aldosteronismo sugiere
que o bien un diagnóstico equivocado o se ha hecho que las complicaciones
asociadas, como la insuficiencia renal o cardiaca, están presentes.
CONSIDERACIONES DIAGNÓSTICAS
Se debe considerar el diagnóstico de aldosteronismo
primario en todas las personas con hipertensión (HTA) e hipocalemia. Hacer el
diagnóstico correcto puede ser la única forma de lograr un control adecuado de
la presión arterial y, por lo tanto, prevenir las secuelas de una HTA mal
controlada.
Las condiciones a considerar en el diagnóstico
diferencial del aldosteronismo primario incluyen las siguientes:
HTA
HTA maligna
Encefalopatía hipertensiva
Hipocalemia
Alcalosis metabólica
Estenosis de la arteria renal
HTA Renovascular
HTA esencial con baja renina: Constituye aproximadamente
el 40% de la HTA esencial
Masticar tabaco
Intoxicación por carbenoxolona
Síndrome aparente de exceso de mineralocorticoides
(AME)
Varias causas de aldosteronismo secundario: a
diferencia del aldosteronismo primario, estas causas se asocian con niveles
elevados de renina (actividad de renina plasmática)
Síndrome de Chrétien: este raro síndrome se
caracteriza por un exceso de mineralocorticoides y una HTA adrenocortical
secundaria a un adenoma pituitario que produce proopiomelanocortina (POMC) [ 17
]
Tumor suprarrenal secretor de deoxycorticosterone
(DOC)
Isquemia renovascular
Preeclampsia (toxemia del embarazo)
Tumor secretor de renina: estos son tumores raros
que surgen del aparato yuxtaglomerular
Consumo excesivo de regaliz: en esta situación, el
componente de ácido glicirricínico inhibe la 11beta-hidroxiesteroide
deshidrogenasa, lo que altera la conversión de cortisol en cortisona en los
riñones; por lo tanto, el cortisol se une a los receptores mineralocorticoides
y actúa como un mineralocorticoide
Otros trastornos y síndromes genéticos / familiares
seleccionados a considerar incluyen los siguientes:
Síndrome de Gitelman - Esto se debe a un cotransportador
de sodio / cloruro defectuoso (NCCT); es básicamente una tubulopatía perdedora
de sal con aldosteronismo secundario
Síndrome de Barrter: es una fenocopia de al menos 3
defectos genéticos distintos (es decir, hiperactividad del cotransportador de
sodio-dicloruro de potasio [NKCC2], el canal de potasio medular externo renal
[ROMK1] o el canal de cloruro epitelial renal [ClCKb], este último codificado
por el gen barttin, también es una tubulopatía que pierde sal con
aldosteronismo secundario y es fisiopatológicamente similar al síndrome de
Gitelman
Síndrome de Gordon: esto se debe a mutaciones
inactivantes de las serina-treonina quinasas WNK1 y WNK4 ("sin lisina
[K]" quinasas), lo que provoca hipertensión, hipercalemia, hipercloremia
leve, acidosis y actividad suprimida de la renina plasmática
Pseudoaldosteronismo (síndrome de Liddle): este es
un trastorno autosómico dominante raro debido a mutaciones hiperactivantes del
canal de sodio epitelial renal (ENaC), con una reabsorción excesiva de sodio en
el túbulo distal renal; los niveles de renina y aldosterona son bajos
Deficiencia de 11beta-hidroxiesteroide
deshidrogenasa
Resistencia a glucocorticoides: esto se debe a
mutaciones inactivantes del receptor de glucocorticoides
DIAGNÓSTICOS DIFERENCIALES
Carcinoma suprarrenal
Incidentaloma suprarrenal
Cirugía suprarrenal
Síndrome de Bartter
Deficiencia de hidroxilasa C-11
Deficiencia de hidroxilasa C-17
Complejo de Carney
Síndrome de Conn
Eclampsia
Síndrome de Cushing Iatrogénico
CONSIDERACIONES DIAGNÓSTICAS
Los individuos con aldosteronismo primario pueden
presentar alcalosis metabólica hipopotasémica; sin embargo, hasta el 38% de los
pacientes con aldosteronismo primario pueden ser normocalémicos al momento de
la presentación. [ 12 ]
Los estudios de laboratorio de rutina pueden mostrar
hipernatremia, hipocalemia y alcalosis metabólica como resultado de la acción
de la aldosterona en el túbulo contorneado distal renal (mejora la reabsorción
de sodio y la excreción de iones de potasio y de hidrógeno). [ 18 ]
PRUEBAS HISTÓRICAS
FLEBOGRAFÍA SUPRARRENAL
Este procedimiento se intentó en la década de 1980 y
su objetivo era visualizar de forma invasiva los patrones venosos que rodean a
los adenomas adrenocorticales. El procedimiento ha caído en descrédito debido
al riesgo de infarto suprarrenal y ya no se usa.
Ensayo terapéutico de espironolactona (Aldactone)
Este procedimiento ya no se usa como una prueba de
diagnóstico para aldosteronismo primario, porque existen alternativas más
fáciles y más rápidas; por lo tanto, actualmente tiene un valor histórico.
Por incompleto, el ensayo terapéutico con
espironolactona involucró la administración de espironolactona por vía oral a
una dosis de 100 mg 4 veces al día durante 5 semanas ya no se usa. Una prueba
positiva se caracterizaría por una disminución en la presión arterial
diastólica de al menos 20 mm Hg.
PRUEBAS DE DETECCIÓN (PRIMER NIVEL)
NIVELES SÉRICOS DE POTASIO Y BICARBONATO
La hipopotasemia y la alcalosis metabólica tienen
bajas sensibilidades y especificidades para el aldosteronismo primario cuando
estos niveles se prueban por sí mismos. La hipopotasemia ( nivel sérico de
potasio menor de 3.6 mEq / l) tiene una sensibilidad del 75-80% mientras el
paciente sigue una dieta normal de sodio. [ 5 ] Por lo general, se asocia con
alcalosis metabólica leve (niveles séricos de bicarbonato mayores de 31 mEq /
l) y una kaliuresis inadecuada (excreción urinaria de potasio mayor de 30 mmol
/ día).
NIVELES DE SODIO Y MAGNESIO
La hipernatremia sérica leve en el rango de 143-147
mEq / L y la hipomagnesemia leve por pérdida renal de magnesio son otros
hallazgos bioquímicos asociados en el aldosteronismo primario establecido. [ 19
]
RELACIÓN DE ACTIVIDAD PLASMÁTICA DE ALDOSTERONA /
RENINA PLASMÁTICA
Dado a que la relación aleatoria de la actividad
plasmática de aldosterona / renina plasmática (PRA) es bastante constante en
muchas condiciones fisiológicas, puede utilizarse para el cribado. Los valores
normales son menores a 270 cuando la concentración de aldosterona se expresa en
pmol / L, o son menores de 10 cuando la concentración de aldosterona se expresa
en ng / dL. [ 20 ]
ALGORITMO 1.
PARA LA DETECCIÓN DE POTENCIAL ALDOSTERONISMO PRIMARIO.
Cuando la aldosterona se mide en ng / dL y la ARP se
mide en ng / ml / h, una relación de aldosterona en plasma / ARP superior a
20-25 tiene una sensibilidad del 95% y una especificidad del 75% para el
aldosteronismo primario. Cuando la aldosterona se mide en pmol / l, una
relación mayor a 900 es consistente con el aldosteronismo primario. [ 21 , 22 ]
LIMITACIONES
Las limitaciones en la utilidad de la ración de
aldosterona / ARP en plasma incluyen lo siguiente:
Una de las principales limitaciones de estas pruebas
es la variabilidad inherente de la secreción de aldosterona debido a un ritmo
circadiano intrínseco
La mayoría de las recomendaciones sugieren realizar
la prueba mientras se retiran todos los antihipertensivos que pueden afectar el
sistema renina-angiotensina (RAS); esto puede ser difícil de lograr cuando una
enfermedad grave dicta la continuación de algunos medicamentos para controlar
la hipertensión (HTA) y la hipopotasemia durante la prueba.
La obtención de la relación aldosterona / ARP en
plasma en el contexto del uso crónico de un inhibidor de la enzima convertidora
de angiotensina (ACE) (es decir, más de 4 semanas de uso) aumenta la
especificidad de la prueba de relación pero reduce la sensibilidad
Aunque la utilidad de las pruebas de la proporción
plasmática de aldosterona / ARP ha sido bien validada en blancos y asiáticos,
no se ha validado en otros grupos raciales importantes.
INTERFERENCIA POR MEDICACIÓN
La relación de aldosterona / ARP en plasma no debe
calcularse cuando el paciente toma medicamentos que pueden interferir con esta
medición. La espironolactona, un antagonista del receptor de aldosterona, debe
suspenderse durante 6 semanas antes de la prueba. Eplerenona, otro antagonista
del receptor de aldosterona, también puede interferir con las pruebas y se debe
suspender durante al menos 2 semanas antes de la prueba.
Los alfabloqueantes, como la doxazosina, no interfieren
con la relación AP / ARP. Los betabloqueantes y los bloqueadores de los canales
de calcio no afectan la precisión diagnóstica de la relación en la mayoría de
los casos.
ARP DESPUÉS
DEL AGOTAMIENTO DE LA SAL Y AGUA Y /
O POSTURA ERGUIDA
En el aldosteronismo primario, la ARP es inferior a
1 ng / ml / hy no aumenta más de 2 ng / ml / h después del agotamiento de la
sal y el agua, la administración de furosemida o 4 horas de postura erecta. Esta prueba, junto con las
pruebas de supresión de captopril, se ha usado como una prueba de detección o
como una prueba confirmatoria (de segundo nivel) para el aldosteronismo
primario.
Las pruebas de confirmación se basan en el concepto
de que la aldosterona se secreta de forma no regulada en el aldosteronismo
primario y, por lo tanto, no puede ser suprimida por las aportaciones
habituales de la regulación fisiológica. De manera similar, la ARP se suprime
crónicamente y tónicamente y no se puede estimular
PRUEBAS DE SUPRESIÓN DE CAPTOPRIL Y LOSARTÁN
Esto implica la administración oral de una sola
dosis de captopril (25-50 mg), un inhibidor de la ECA. En individuos sanos, los
niveles de aldosterona se suprimirán a menos de 15 ng / dL. La prueba tiene una
sensibilidad de 90-100% pero una especificidad de solo 50-80%.
En un estudio de 135 pacientes que se sometieron a
las pruebas de captopril y losartán (bloqueador de los receptores de
angiotensina-II [ARB]), Wu et al concluyeron que los valores de la relación de
ARP y la concentración de aldosterona derivada de la prueba de losartan eran
más precisos que los obtenidos mediante la prueba de captopril para el
diagnóstico de aldosteronismo primario. [ 23 ]
Los autores encontraron que cuando se utilizaba una
relación de ARP (ng / dL por ng / ml / h) superior a 35 y una concentración de
aldosterona de más de 10 ng / dL, los valores de especificidad diagnóstica para
captopril y losartan eran 89.1% y 93.8 %, respectivamente, y los valores de
sensibilidad de diagnóstico respectivos fueron 66.2% y 84.5%. Los autores
recomiendan la realización preferencial de la prueba de supresión de losartán.
PRUEBAS DE CONFIRMACIÓN (SEGUNDO NIVEL)
NIVEL DE ALDOSTERONA SÉRICA
Después de 3 días de una dieta sin restricción de
sodio y 1 hora de decúbito horizontal, las personas sanas tienen niveles de
aldosterona de menos de 15 ng / dL. Cuando la aldosterona sérica se eleva por
encima de 22 ng / dl y se suprime la renina, la prueba de aldosterona sérica (S-Aldo)
prácticamente confirma el diagnóstico de aldosteronismo primario. Sin embargo,
debido a que la secreción de aldosterona es variable, el valor predictivo
negativo y positivo de un único nivel aleatorio de aldosterona es limitado.
Hasta un 40% de los pacientes con aldosteronismo
primario tienen niveles séricos de aldosterona que permanecen dentro del rango
de referencia en las pruebas repetidas, como suele ser el caso en la
hipertensión esencial (HTA). (Vea la tabla a continuación).
Algoritmo para la confirmación de aldosteronismo primario (ALGORITMO 2)
PRUEBA DE EXCRECIÓN URINARIA DE ALDOSTERONA EN 24
HORAS
La prueba de excreción urinaria de aldosterona (Aldo-U)
es una de las herramientas diagnósticas confirmatorias más útiles porque es un
índice para la secreción diaria total de aldosterona (de manera similar al cortisol
libre de orina de 24 h [CLU]) el cual está
típicamente elevado en pacientes con síndrome de Cushing).
En la mayoría de los pacientes con aldosteronismo
primario, el Aldo-U de 24 horas es mayor que 14 mcg / día (después de 3 días de
carga de sal). Solo alrededor del 7% de los pacientes con aldosteronismo
primario tienen valores de menos de 14 mcg / día.
PRUEBA DE CARGA DE SAL
La prueba de carga de sal puede realizarse
utilizando un protocolo de carga de sal intravenosa o un protocolo de carga de
sal oral. El protocolo oral requiere la ingestión diaria de al menos 10-12 g de
cloruro de sodio durante al menos 5 días antes de realizar la prueba. Cuando se
ha cumplido el protocolo oral, se miden las excreciones Aldo-U, sodio, potasio
y creatinina durante 24 horas, y se debe determinar la aldosterona sérica y la
ARP. En individuos normales, el principal metabolito de Aldo-U, la
aldosterona-18-glucurónido urinario, debe caer por debajo de un nivel de 17 mcg
/ día. La no supresión de Aldo-U-18G es altamente sugestiva de aldosteronismo
primario. No obstante, esta prueba es engorrosa y rara vez se realiza.
La medición de creatinina urinaria de 24 horas
valida la idoneidad de la muestra de orina, mientras que un valor de sodio
urinario de 24 horas de al menos 250 mEq / día confirma una carga de sal
adecuada durante los días previos a la prueba y, por lo tanto, valida las otras
mediciones.
DETERMINACIÓN DE LAS PRUEBAS DEL SUBTIPO DE ALDOSTERONISMO
PRIMARIO (TERCER NIVEL)
Una vez que se ha confirmado el diagnóstico de
aldosteronismo primario mediante una prueba de primer o segundo nivel, el
siguiente paso es determinar el subtipo de aldosteronismo primario e
identificar una enfermedad curable quirúrgicamente. A efectos prácticos, esto
significa distinguir entre un adenoma suprarrenal y una hiperplasia suprarrenal
idiopática (HAI). (Ver el cuadro a continuación) [ 18 , 24 ]
Algoritmo para distinguir subtipos de aldosteronismo
primario. (ALGORITMO 3)
En general, los pacientes con adenomas son más
jóvenes que los pacientes con hiperplasia y tienen hipertensión (HTA) e
hipopotasemia más severa, así como niveles más altos de aldosterona en la orina
(Aldo-U) que los pacientes con HAI. Sin embargo, estos parámetros clínicos no
son lo suficientemente confiables para distinguir con precisión el adenoma de
la HAI
PRUEBA DE ESTIMULACIÓN POSTURAL
Los aldosteronomas se asocian con una disminución
anómala del nivel de aldosterona con la postura erguida, en contraste con los
pacientes con hiperplasia suprarrenal idiopática (HAI), en los que se produce
un aumento del nivel de aldosterona mediado por el sistema renina angiotensina
(RAS) con la postura erguida.
De forma similar, se produce un aumento del nivel de
aldosterona sérica en pacientes con adenomas sensibles a renina (ASR), HTA
esencial de baja renina y casos muy raros de hiperplasia suprarrenal unilateral
(este último presenta características intermedias entre la hiperplasia
suprarrenal idiopática [IAH] y la aldosterona). produciendo adenoma
suprarrenal, ocasionalmente designado como "aldosteronismo
intermedio"). [ 25 ]
Cuando la tomografía abdominal (TC) y la resonancia
magnética (RM) se combinan con estimulación postural, el valor predictivo positivo
(VPP) de una prueba postural anormal en la predicción de aldosteronismo
primario corregible quirúrgicamente debido a un solo adenoma es del 98%.
El protocolo de prueba postural estándar implica la
obtención de valores iniciales para los niveles de aldosterona sérica (Aldo-S)
y actividad de renina plasmática (ARP), así como estos niveles 2 horas después
de que el paciente haya asumido una postura erguida. Los niveles de Aldo-S
típicamente aumentan en esta configuración al menos un 50% por encima del valor
inicial en personas sanas, en personas con HTN esencial y en el subgrupo de
pacientes con aldosteronismo primario que tienen hiperplasia suprarrenal
idiopática (HAI) o ASR.
Entre los pacientes con aldosteronomas (adenomas
productores de aldosterona, APA), los niveles de S-Aldo generalmente no
aumentan o, paradójicamente, descienden a este nivel. Se ha informado que la
sensibilidad y especificidad de esta prueba en el diagnóstico diferencial de
las principales causas del aldosteronismo primario es tan alta como 80-85%.
PRUEBA DE ESTIMULACIÓN DE FUROSEMIDA (LASIX)
Esta prueba a menudo se combina con la prueba de
postura erguida. La prueba típica implica la administración oral de 40 mg de
furosemida la noche anterior, así como la mañana de la prueba. En la mañana de
la prueba, después de que se haya administrado la dosis de furosemida, el
paciente permanece en posición vertical de 2 a 3 horas; luego, se analizan los
niveles de Aldo-S y ARP. La interpretación de los resultados de la prueba es
similar a la descrita anteriormente para la prueba de estimulación postural.
RITMO DIURNO DE LA ALDOSTERONA
El ritmo circadiano de la secreción de aldosterona
en individuos sanos es similar al del cortisol y depende de la corticotropina.
Los valores más bajos se observan alrededor de las 11:30 p.m. hasta la
medianoche, y los valores más altos ocurren temprano en la mañana alrededor de
las 7: 30-8: 00 a.m. (suponiendo un ciclo normal de sueño-vigilia). Si bien
esto se conserva en pacientes con aldosteronomas, generalmente se pierde en
pacientes con HAI.
En algunos pacientes con aldosteronomas se pueden
encontrar niveles elevados de corticosterona 18OH y / o cortisol 18OH en plasma
y orina, pero son poco frecuentes en la HAI. [ 26 , 27 ]
TOMOGRAFÍA COMPUTADA Y RESONANCIA MAGNÉTICA NUCLEAR
TC
La investigación radiológica inicial en el estudio
del aldosteronismo primario es una tomografía computada suprarrenal de alta
resolución y corte fino (2-2.5 mm) con contraste.
Los aldosteronomas tienden a ser pequeños, en contraste
con los adenomas adrenocorticales productores de cortisol; solo los
aldosteronomas que tienen al menos 1 cm de diámetro se pueden detectar de
manera confiable y consistente.
La sensibilidad general de la tomografía computada
suprarrenal de alta resolución y corte fino es mayor al 90%, pero la imagen se
complica por los muchos hallazgos falsos positivos asociados con los
incidentalomas, que se informan en algunas series que se encuentran hasta en
10- 15% de la población general (su prevalencia aumenta con la edad). [ 28 ]
Además, los estudios con TC de alta resolución en
realidad pueden ser perjudiciales, ya que estas exploraciones a menudo detectan
la hiperplasia que acompaña a los adenomas y pueden dar lugar a una tendencia a
sobrediagnosticar la hiperplasia suprarrenal idiopática (HAI). De manera
similar, debido a que la hiperplasia suprarrenal a largo plazo se asocia con la
formación de pseudonódulos y nódulos, esta imagen radiográfica a menudo se
puede confundir con el diagnóstico de adenomas autónomos.
INDICACIONES QUIRÚRGICAS
Algunos investigadores sugieren que cuando se
detecta un macroadenoma unilateral solitario (mayor de 1 cm) en una tomografía
computarizada en un paciente joven en el contexto de un aldosteronismo
inequívoco, está indicada la adrenalectomía unilateral. Sin embargo, debido al
riesgo dependiente de la edad de que un macroadenoma suprarrenal unilateral
solitario pueda ser un adenoma no funcional, algunos expertos creen que el
muestreo de la vena suprarrenal [ 18 ] debe realizarse en pacientes mayores de
40 años.
RMN
En general, se acepta que la RMN no es superior a la
TC con contraste para la visualización adrenal. Las tomografías computarizadas
de alta resolución en realidad pueden tener una mejor definición suprarrenal.
Figura 1 Imagen de resonancia magnética (RMN) en un
paciente con síndrome de Conn que muestra un adenoma suprarrenal izquierdo.
Si el examen (de TC y RMN) de un paciente con
aldosteronismo primario es completamente normal, generalmente se recomienda un ensayo
de tratamiento de 6 a 12 meses con antagonistas de aldosterona, después de lo
cual los estudios de imágenes deben repetirse. El tratamiento con
glucocorticoides también se puede considerar para el aldosteronismo remediable
con glucocorticoides (GRA), si se sospecha esta condición.
GAMMAGRAFÍA NP-59 IODO-METIL-NORCOLESTEROL
Aunque es bastante difícil de configurar y no está
disponible de forma rutinaria, esta prueba puede ser útil en casos
seleccionados para distinguir entre adenomas e hiperplasia. En los grandes
centros de referencia de medicina nuclear, el valor discriminante de la prueba
se aproxima al de la muestra venosa suprarrenal (cerca del 90%), especialmente
con tumores más grandes de 1,5 cm de diámetro o más. La actividad típica
administrada es de 37 MBq (1 miliCurie; mCi).
Figura 2 Escintigrama obtenido mediante el uso de
yodo-131-beta-yodo
El escintigrama obtenido mediante el uso de
yodo-131-beta-yodometil-norcolesterol (NP-59) en un hombre de 59 años con
hipertensión muestra una captación de radionúclidos bastante intensa en el
tumor adrenal derecho. En la cirugía, se confirmó un tumor de Conn.
Los resultados de la prueba mejoran si ha habido una
supresión previa con dexametasona de las glándulas suprarrenales usando 0,5-1
mg de dexametasona oral cada 6 horas. En este contexto, las imágenes de adenoma
permanecen visibles, mientras que las imágenes de glándulas hiperplásicas se
desvanecen después de 2-3 días de tratamiento con dexametasona.
La exploración estándar puede producir un resultado
falso negativo para aldosteronomas pequeños; sin embargo, el rendimiento
diagnóstico se puede aumentar mediante la administración conjunta de
espironolactona. Esta es la principal alternativa de diagnóstico para el
muestreo venoso suprarrenal (AVS).
Un estudio retrospectivo de Di Martino et al indicó
que, en casos seleccionados, el aldosteronismo primario puede localizarse
preoperatoriamente mediante la prueba NP-59 en lugar del muestreo venoso
adrenal. Basando el rendimiento de la prueba en los resultados patológicos, la
sensibilidad y el valor predictivo positivo fueron 90.9% y 83.3%,
respectivamente; basar el rendimiento en el control de la presión arterial
postoperatoria resultó en una sensibilidad y un valor predictivo positivo del
91,6% (para ambos). [ 29 ]
MUESTREO VENOSO SUPRARRENAL
Debido a que este procedimiento depende en gran
medida de la disponibilidad de radiólogos intervencionistas técnicamente
competentes, no puede (y no debe) realizarse universalmente, a pesar de que es
el criterio estándar para la confirmación del exceso de aldosterona
lateralizable. [ 30 , 31 , 32 ]De hecho, el muestreo de la vena suprarrenal
puede realizarse selectivamente solo cuando las imágenes preoperatorias no
pueden lateralizar definitivamente un aldosteronoma supuestamente unilateral.
Un informe de Dekkers et al apoya esta línea de argumentación y cuestiona la
noción de realizar muestreo venoso adrenal en todos los pacientes con
aldosteronismo primario. El estudio encontró que en el seguimiento de un año, la
intensidad de la medicación hipertensiva y los beneficios clínicos no
difirieron significativamente entre los pacientes evaluados por muestreo venoso
suprarrenal y los evaluados por TC suprarrenal. [ 33 ]
El muestreo venoso suprarrenal probablemente tenga su
mayor utilidad cuando los hallazgos de imágenes suprarrenales son completamente
normales a pesar de la evidencia bioquímica de aldosteronismo primario y en
entornos en los que la patología suprarrenal bilateral está presente en las
imágenes y la bioquímica sugiere la presencia de un aldosteronoma funcional.
La prueba también tiene utilidad para resolver la
etiología exacta en casos de aldosteronismo primario en el que existe
discordancia entre los hallazgos bioquímicos y los hallazgos radiológicos con
respecto a si el aldosteronismo primario se debe a una hiperplasia suprarrenal
idiopática (HAI) o un aldosteronoma.
Una serie informó que el 41% de los pacientes con
una tomografía computada suprarrenal normal que tenían evidencia bioquímica de aldosteronismo
primario en realidad tenían enfermedad lateralizable, mientras que el 49% de
los pacientes con micronódulos bilaterales en la tomografía computarizada
también tenían enfermedad lateralizable. [ 34 ] Incluso en los casos en los que
solo se encontró un solo nódulo suprarrenal en las imágenes, cuando se realizó
un muestreo venoso suprarrenal, confirmó una enfermedad lateralizable en solo
el 51-66% de los casos.
Técnica
Las venas suprarrenales se cateterizan a través de
un abordaje venoso femoral percutáneo. Los catéteres venosos derecho e
izquierdo deben colocarse en las venas suprarrenales ipsilaterales para evitar
errores en el manejo de las muestras. (La canulación de la vena suprarrenal
derecha es técnicamente difícil debido a la corta longitud de este vaso. La
vena suprarrenal izquierda es más larga, lo que permite una colocación más
estable del catéter).
Al inicio y después de la estimulación con
corticotropina (preferiblemente mediante infusión continua a 50 mcg / h durante
la duración del estudio de muestreo), se obtienen muestras de sangre
simultáneamente de ambas venas suprarrenales, así como de la vena cava
inferior, y las muestras se analizan para aldosterona y cortisol.
Con el fin de documentar la colocación de los
catéteres dentro de las venas suprarrenales, se calcula una relación de
cortisol adrenal a vena cava (post corticotropina); debe ser mayor que 5-10.
DIAGNÓSTICO
La precisión de la prueba excede el 95% cuando el
procedimiento es técnicamente exitoso. Si la secreción unilateral autónoma de
aldosterona está presente en cualquier lado, la relación de las concentraciones
de aldosterona entre las venas suprarrenales derecha e izquierda generalmente
excede 10: 1. Se pueden presentar resultados falsos positivos cuando la estenosis
de la arteria renal está presente; por lo tanto, la estenosis de la arteria
renal debe excluirse completamente, especialmente antes de realizar una prueba
altamente invasiva.
La mayoría de los pacientes con una fuente
unilateral de aldosterona tienen relaciones de aldosterona adrenal a cortisol
suprarrenales superiores a 4. Las relaciones de menos de 3 sugieren
hiperplasia, y los valores de 3-4 se consideran resultados indeterminados.
Riesgos
El muestreo venoso suprarrenal no está exento de
riesgos. La trombosis venosa suprarrenal e ilíaca, la hemorragia suprarrenal,
la insuficiencia suprarrenal o incluso la hemorragia venosa mayor debido a
desgarros transmurales y luxaciones del catéter se encuentran entre las
posibles complicaciones.
ENSAYOS DE HIDROXICORTICOSTERONA Y
OXOCORTISOL-HIDROXICORTISOL
Debido a las diferentes zonas adrenocorticales
implicadas en la hiperplasia idiopática, en comparación con los adenomas, los
ensayos de plasma 18-hidroxicorticosterona (18-OHB) o plasma y / orina
18-oxocortisol (18-oxo-F) / 18-hidroxicortisol pueden ser de uso diagnóstico [ 26 , 27 ]
5MED
Esteroides adrenocorticales de la zona de
transición.
Los aldosteronomas suelen estar asociados con
niveles de 18-OHB superiores a 100 ng / dL. De manera similar, el
aldosteronismo remediable por glucocorticoides (GRA, hiperaldosteronismo
familiar de tipo 1), aunque es una enfermedad hiperplásica por definición,
también se asocia con una producción incrementada de estos derivados de 18-oxo
/ hidroxi. Esta distinta bioquímica no está presente en los adenomas sensibles
a la renina (RRA). En este punto, pocos centros envían estas pruebas
especializadas de bioquímica, y su valor actual es principalmente histórico
PRUEBA DE SUPRESIÓN DE FLUDROCORTISONA
Esta prueba funciona según el mismo principio en que
se basan la infusión intravenosa de cloruro de sodio o las pruebas de carga
oral de sal para confirmar el diagnóstico de aldosteronismo primario. Sin
embargo, la prueba de supresión de la fludrocortisona ha perdido gran parte de
su popularidad, ya que requiere hospitalización del paciente y de 4 a 5 días
para completarse, y actualmente es principalmente de interés histórico.
Por razones de compleción, la descripción de esta
prueba es la siguiente: la fludrocortisona se administra por vía oral a una
dosis de 0.1-0.2 mg cada 6 horas, junto con cloruro de sodio y potasio
suplementarios. En el individuo sano, después de esta estimulación, el nivel
sérico de aldosterona (S-Aldo) se suprime típicamente a menos de 8 ng / dl, con
una excreción urinaria de aldosterona (U-Aldo) menor de 12 mcg / día.
En pacientes con aldosteronismo primario, ni el
nivel de aldosterona en orina ni el nivel de aldosterona en plasma suprime los
umbrales mencionados anteriormente.
PRUEBA DE SUPRESIÓN DE DEXAMETASONA
Esta prueba es relevante solo en el contexto de un
posible aldosteronismo familiar. Habitualmente, en pacientes con aldosteronismo
primario, la dexametasona se asocia con una reducción transitoria de leve a
moderada de los niveles de aldosterona en plasma y urinaria, aunque no en el
rango de referencia normal. [ 7 ]
En el subgrupo de pacientes con aldosteronismo
primario con aldosteronismo remediable con glucocorticoides (GRA), dosis
pequeñas de dexametasona (1-2 mg / día) inducen la normalización completa en
los niveles plasmáticos y de aldosterona en la orina. Esto está invariablemente
asociado con una mejoría en la hipertensión (HTA) en estos pacientes. Otros
informes sugieren un nivel de corte para la aldosterona plasmática de menos de
4 ng / dL y / o una supresión relativa de aldosterona en plasma de más del 80%
de la línea de base para el diagnóstico de GRA después del desafío con
dexametasona.
Existen tres variantes del aldosteronismo primario
familiar. El aldosteronismo primario familiar tipo 1 (también llamado GRA) se
relaciona con la mejoría de la HTA con dosis bajas de dexametasona. Los
aldosteronismos primarios familiares tipo 2 y 3 no son suprimibles con
dexametasona.
PRUEBA DE METOCLOPRAMIDA (REGLAN)
Esta es una prueba no invasiva para distinguir entre
aldosteronomas e hiperplasia suprarrenal idiopática (IAH). Aprovecha la
expresión diferencial de los receptores de dopamina en la membrana celular de
las células adrenocorticales.
En condiciones normales, la dopamina causa la
inhibición tónica de la aldosterona, mientras que la serotonina (5-HT) provoca
una mayor secreción de aldosterona in vivo. La metoclopramida es un antagonista
del receptor de la dopamina D2, así como un agonista parcial del receptor 4 de
la serotonina (5-HT4) y, por lo tanto, su administración conduce a un aumento
de los niveles de aldosterona. Este patrón normal de respuesta se retiene en
pacientes con aldosteronomas e hipertensión de baja renina (HTN), pero no en
pacientes con HAI. [ 35 ]
Después de una inyección intravenosa de 10 mg de
metoclopramida, los niveles séricos de aldosterona aumentan significativamente
en pacientes con aldosteronomas, pero permanecen sin cambios o paradójicamente
reducidos en pacientes con HIA. Esta prueba experimentó un aumento en el uso a
mediados de la década de 1990, especialmente en Europa, pero actualmente se usa
muy poco en los Estados Unidos.
ESTUDIOS DE LABORATORIO ADICIONALES
PRUEBA DE ESTIMULACIÓN DE CORTICOTROPINA
La prueba de estimulación con corticotropina usa la
inyección intravenosa estándar de 250 mcg. En aldosteronomas, típicamente se
observa una respuesta robusta de aldosterona. En la hiperplasia suprarrenal
idiopática (HAI), la oleada de aldosterona es considerablemente más débil. La
prueba ya no se usa porque el valor discriminante de la prueba es bastante
pobre. [ 6
PRUEBA DE INFUSIÓN DE ANGIOTENSINA II
Esta prueba implica evaluar la respuesta de la
actividad de la renina plasmática (ARP) y la aldosterona sérica (Aldo-S) a una
infusión continua de angiotensina II. Las características de respuesta son
similares a las observadas en las pruebas de postura, con un aumento apropiado
en el nivel de aldosterona observado en HAI pero no en aldosteronomas.
La prueba de infusión de angiotensina II es mucho
menos popular que otras pruebas de aldosteronismo porque requiere infusión
continua y monitorización hemodinámica cercana, y rara vez se usa hoy en día.
HALLAZGOS HISTOLÓGICOS
Los hallazgos histológicos varían de acuerdo con el
tipo de aldosteronismo primario que tiene un paciente. Los aldosteronomas
típicos se caracterizan por tejido adenomatoso, generalmente con morfología de
tipo zona fasciculada. La mayoría de estos tumores son pequeños (<3 a="" acinos="" asociada="" c="" cargadas="" cm="" cordones.="" de="" di="" difusa="" dispuestas="" en="" focal="" hiperplasia="" l="" la="" las="" lulas="" mayor="" menudo="" metro="" o:p="" o="" ocurre.="" pidos="" son="" y="">
Los adenomas sensibles a la renina (RRA) se
caracterizan por una morfología de tipo zona glomerulosa. Las únicas otras
características distintivas son características bioquímicas únicas y
predecibles.
La hiperplasia suprarrenal idiopática (IAH) se
caracteriza por hiperplasia difusa que puede ser micronodular, macronodular o
una mezcla de ambas. La morfología de las células es comúnmente similar a la
zona glomerulosa.
En la hiperplasia suprarrenal primaria (HAP),
típicamente se observa hiperplasia difusa, que es unilateral y tiene morfología
de la zona fasciculada.
El síndrome de aldosteronismo primario rara vez
ocurre en el contexto del carcinoma suprarrenal, por lo que la causa de la
hipersecreción de aldosterona es una enfermedad maligna (en lugar de un adenoma
benigno). En tales casos, la histopatología revela las características típicas
del carcinoma adrenocortical (CCA) , incluidas las figuras mitóticas, la invasión
local y las metástasis ganglionares locorregionales.
TRATAMIENTO
Consideraciones de enfoque
Entre los principales objetivos del tratamiento para
el aldosteronismo primario se encuentran (1) la normalización de la presión
arterial, (2) la normalización de los niveles de potasio sérico y otros
electrolitos, y (3) la normalización de los niveles séricos de aldosterona. [
18 , 36 ]
El tratamiento apropiado para el aldosteronismo
primario depende de su causa. Aunque la hipertensión (HTA) se cura frecuentemente
después de una adrenalectomía unilateral en pacientes con aldosteronismo
primario secundario a un aldosteronoma suprarrenal, la tasa media de curación
de la HTA es solo del 19% después de una suprarrenalectomía unilateral o
bilateral en pacientes con hiperplasia suprarrenal idiopática (HAI). Por lo
tanto, el tratamiento médico es el tratamiento de elección para la variante HAI
de aldosteronismo primario.
MED
Efectos de los principales antihipertensivos en el
sistema renina-angiotensina.
En pacientes con un aldosteronoma, el tratamiento
médico se usa preoperatoriamente para controlar la presión arterial y corregir
la hipocalemia, disminuyendo así el riesgo quirúrgico. La terapia médica
también se administra a pacientes con HTA persistente en el postoperatorio,
candidatos quirúrgicos pobres y pacientes que rechazan la cirugía.
En pacientes con insuficiencia cardíaca que tienen
aldosteronismo secundario, se ha demostrado que el antagonismo de la
aldosterona por espironolactona y eplerenona confiere un beneficio de
supervivencia. [ 37 ]
TERAPIA FARMACOLÓGICA
BLOQUEADORES DE LOS CANALES DE CALCIO
Al inhibir el flujo de calcio intracelular en las
células adrenocorticales, los bloqueadores de los canales de calcio
dihidropiridínicos reducen la producción de aldosterona en respuesta a una
variedad de estimulantes, que incluyen potasio, corticotropina y
angiotensina-II.
La nifedipina es la más ampliamente estudiada de
estos medicamentos; sin embargo, aunque la nifedipina causa una mejoría
significativa en pacientes con hipertensión (HTA), no aborda la fisiopatología
de la afección. La actividad de la renina plasmática (ARP), los niveles de
aldosterona, el volumen plasmático y las concentraciones séricas de potasio
permanecen esencialmente sin cambios mientras se usa nifedipina.
ANTAGONISTAS DE MINERALOCORTICOIDES
Los antagonistas de mineralocorticoides, como la
espironolactona, son ligandos inhibidores del receptor mineralocorticoide (MR).
Logran un notable control de la presión arterial y la normalización del volumen
plasmático y las concentraciones séricas de potasio, particularmente en
pacientes con aldosteronomas. [ 38 ]
Los efectos saludables de la espironolactona parecen
deberse principalmente a su impacto en el equilibrio de la sal y el agua en
lugar de su antagonismo de la aldosterona en el riñón. La combinación de
espironolactona y tiazidas a menudo proporciona un mejor control de la presión
arterial que la espironolactona sola.
Debido a los efectos adversos estrógenos de la espironolactona,
incluida la impotencia y la ginecomastia, el incentivo para desarrollar un
agente antialdosterónico de eficacia similar sin estos efectos adversos es
considerable. La eplerenona es un agente antialdosterónico selectivo que puede
cumplir esta promesa, ya que es un antagonista específico del receptor de la
aldosterona que no tiene los efectos antiandrógenos adicionales asociados con
la espironolactona.
GLUCOCORTICOIDES
En el subgrupo de pacientes con aldosteronismo
remediable con glucocorticoides (GRA), el tratamiento de elección es la
administración de la dosis más baja posible de glucocorticoides que se puede
usar para lograr un control adecuado de la presión arterial. Debido a los
posibles efectos adversos que pueden resultar incluso de un exceso sutil de
glucocorticoides, el uso de glucocorticoides de acción corta, como la
prednisona y la hidrocortisona (en lugar de la dexametasona), generalmente es
lo mejor.
OTROS
Los inhibidores de la ECA y los bloqueadores de los
receptores de angiotensina (BRA) también son opciones de tratamiento
potenciales. Las opciones de tratamiento médico menos ideales incluyen
diuréticos ahorradores de potasio, como triamtereno y amilorida, que no son
antagonistas de mineralocorticoides. La amilorida actúa a nivel del túbulo
contorneado distal pero no se une a los receptores mineralocorticoides.
Existen algunos informes del uso de inyección
percutánea de etanol o ácido acético en aldosteronomas como una modalidad de
tratamiento; en estos casos, el tratamiento generalmente se administró a
pacientes para quienes la cirugía estaba contraindicada. [ 39 ] Esta técnica no
es popular ni está bien validada. Además, requiere la experiencia técnica de un
radiólogo intervencionista altamente capacitado.
CONSIDERACIONES
La terapia no quirúrgica también es una opción de
tratamiento viable en pacientes que tienen enfermedad lateralizable pero que
son candidatos quirúrgicos pobres debido a otras comorbilidades coexistentes.
También es una opción de tratamiento viable en el raro entorno de los adenomas
suprarrenales funcionales bilaterales que de otra manera requerirían una
adrenalectomía bilateral.
CIRUGÍA SUPRARRENAL
La cirugía es el tratamiento de elección para las
variantes lateralizables del aldosteronismo primario, incluidos los
aldosteronomas típicos, los adenomas sensibles a la renina (RRA) y la
hiperplasia suprarrenal primaria (HAP).
Preoperatoriamente, una vez que se hayan realizado y
confirmado los diagnósticos bioquímicos y anatómicos, el paciente debe comenzar
un ciclo de espironolactona de 3 a 5 semanas. Esto sirve como una herramienta
de diagnóstico adicional (para confirmar el diagnóstico de aldosteronismo
primario) y como un medio para predecir la respuesta de la presión arterial que
se puede esperar después de la cirugía.
Una adrenalectomía se puede realizar a través de una
laparotomía formal o mediante el uso de una técnica laparoscópica (con el
rendimiento de este último cada vez más común). La opción laparoscópica ahora
permite ofrecer terapia quirúrgica a pacientes relativamente débiles que no
podrían resistir una laparotomía formal. Los estudios en curso evalúan
sistemáticamente el lugar de las operaciones de conservación suprarrenal frente
a la adrenalectomía unilateral total en estos pacientes. [ 40 ]
Entre las opciones estudiadas se encuentran (1)
suprarrenalectomía parcial, en la que se realiza una resección en cuña de la
glándula con el adenoma junto con enucleación de aldosteronoma y (2)
adrenalectomía ahorradora de médula, en la que se intenta retener la médula
suprarrenal tejido mientras se elimina la corteza.
RESULTADOS
Alrededor del 60-70% de los pacientes se vuelven
normotensos después de la cirugía curativa para aldosteronomas cuando se
evalúan 1 año después de la operación. La hipertensión (HTA) típicamente no se
resuelve inmediatamente después de la operación sino, más bien, durante 3 a 6
meses. (Aunque después de la cirugía, prácticamente todos los pacientes con un
aldosteronoma tienen reducciones significativas en la secreción de aldosterona
y la presión arterial y también demuestran una corrección de la hipopotasemia.
[ 41 , 42 , 43 , 44 , 45 ] )
Un estudio retrospectivo de 168 pacientes con
aldosteronismo primario sometidos a una suprarrenalectomía encontró que la HTA
se curó o controló en el 77% de los pacientes con adenoma unilateral y en el
68% de los pacientes con aldosteronismo que no tenían adenoma, pero cuya
relación aldosterona / cortisol fue al menos 5 veces mayor en el lado dominante
que en el lado no dominante. [ 43 ]
El porcentaje de pacientes que permanecen
normotensos 5 años después de la operación es aproximadamente del 53%. La
resolución de la HTN después de la adrenalectomía ocurre invariablemente en el
contexto de un historial familiar en el que la HTN está ausente y / o cuando el
paciente ha usado preoperatoriamente 2 o menos antihipertensivos.
La adrenalectomía tiene muy poca utilidad en el
contexto de la hiperplasia suprarrenal idiopática (HAI). En los casos
informados en los que se ha realizado cirugía involuntariamente en pacientes
con IAH, los efectos sobre la presión arterial, la hipocalemia y la
hipersecreción de aldosterona han sido mínimos, lo que refuerza aún más la
necesidad de hacer un diagnóstico correcto antes de justificar una
adrenalectomía.
La persistencia de la HTA después del aparente
tratamiento quirúrgico de la enfermedad lateralizable es más común en pacientes
mayores de 45 años, en aquellos que tuvieron HTA durante más de 5 años antes de
la cirugía y en personas que no respondieron antes de la operación a la
espironolactona. [ 43 , 44 ]
La HTA persistente puede estar relacionada con el
restablecimiento de los barorreceptores, los cambios hemodinámicos
establecidos, los cambios estructurales en los vasos sanguíneos o la HTA
esencial coincidente.
Otra posibilidad a considerar en la HTA persistente
es una resección incompleta del adenoma, con tejido remanente hiperplásico
remanente. La coexistencia de nefroesclerosis hipertensiva en algunos pacientes
con HTN persistente también es una posibilidad clara. También se debe
considerar la coexistencia de otras causas secundarias de HTA; la estenosis de
la arteria renal es una consideración importante.
CUIDADO PREOPERATORIO Y POSTOPERATORIO
Antes de la cirugía, los pacientes deben recibir al
menos 8-10 semanas de tratamiento médico para disminuir la presión arterial y
corregir los síndromes metabólicos que a menudo se asocian con el
aldosteronismo primario.
En el postoperatorio, los perfiles metabólicos deben
ser monitoreados de cerca. La mayoría de los pacientes no desarrollan
hipomineralocorticoidismo permanente y, por lo tanto, no requieren reemplazo de
fludrocortisona.
Para los pacientes que desarrollan
hipoaldosteronismo, los síntomas pueden persistir por un tiempo prolongado y
pueden ser similares al retraso observado en la recuperación de
glucocorticoides suprarrenales luego de la supresión crónica de la
corticotropina por esteroides exógenos. Sin embargo, si se desarrolla
hiperpotasemia significativa , se deben suspender los suplementos de potasio y
se puede iniciar el tratamiento con furosemida a dosis de 80 a 160 mg diarios.
DIETA
Una dieta baja en sal, aunque útil para lograr el
control de la presión arterial en el aldosteronismo primario, puede estar
asociada con resultados negativos falsos en las pruebas bioquímicas.
Una dieta alta en sal dificulta el logro del control
de la presión arterial y puede dar resultados falsos positivos en las pruebas
bioquímicas.
RESUMEN DE PAUTAS
Una serie de recomendaciones sobre el manejo del
aldosteronismo primario fueron desarrolladas por la Sociedad Francesa de
Endocrinología (SFE), la Sociedad Francesa de Hipertensión (SFHTA) y la
Asociación de Cirugía Endocrina Francófona (AFCE). [ 46 , 47 , 48 , 49 , 50 ,
51 , 52 , 53 ] Incluyen una recomendación para detectar aldosteronismo primario
en pacientes con cualquiera de los siguientes:
Hipertensión severa (presión arterial sistólica de
180 mm Hg o mayor o presión arterial diastólica de 110 mm Hg o mayor)
Hipertensión resistente (presión arterial sistólica
de 140 mm Hg o superior o presión arterial diastólica de 90 mm Hg o superior,
incluso después del uso de al menos tres agentes antihipertensivos, incluido un
diurético tiazídico)
Hipertensión asociada a hipopotasemia (ya sea
espontánea o diurética asociada)
Hipertensión o hipocalemia relacionada con un
incidentaloma suprarrenal
Con respecto a la cirugía, las recomendaciones
establecen que la adrenalectomía laparoscópica se debe utilizar en pacientes
con aldosteronismo primario lateralizado que son candidatos para cirugía. En
términos de tratamiento médico, se recomienda el uso de amilorida en pacientes
con intolerancia a la espironolactona, mientras que la eplerenona se sugiere
como otra alternativa en casos de intolerancia a la espironolactona o si la
amilorida no controla suficientemente la hipertensión.
En una actualización de 2016 de sus guías de
práctica clínica para el diagnóstico y tratamiento del aldosteronismo primario
de 2008, la Endocrine Society incluyó las siguientes recomendaciones [ 54 , 55
] :
Detección de la condición en sujetos con presión
arterial sostenida superior a 150/100 mm Hg, como se encuentra en cada una de
las tres mediciones obtenidas en días diferentes, así como en pacientes con
hipertensión (presión arterial> 140/90 mm Hg) resistente a tres
convencionales medicamentos antihipertensivos (incluido un diurético) o con
presión arterial controlada (<140 a="" accidente="" aldosteronismo="" antecedentes="" antihipertensivos="" apnea="" cerebrovascular="" con="" cuatro="" de="" debe="" del="" diur="" e="" edad="" el="" en="" espont="" familiares="" grado="" hg="" hipertensi="" hipertensos="" hipocalemia="" incidentaloma="" inducida="" inicio="" los="" m="" medicamentos="" mm="" n="" neos="" o:p="" o="" os="" pacientes="" por="" primario="" primer="" realizar="" s="" se="" sue="" suprarrenal="" tambi="" tamizaje="" temprana="" temprano="" ticos="" todos="" una="" y="">
El uso de la relación aldosterona / renina plasmáticas para la
detección de aldosteronismo primario posible en los grupos de pacientes
anteriores
El uso de una o más pruebas confirmatorias en
pacientes con una relación plasmática positiva de aldosterona / renina para
confirmar o excluir definitivamente el diagnóstico
El uso de tomografía computarizada adrenal en todos
los pacientes con aldosteronismo primario para excluir grandes masas que pueden
representar el carcinoma adrenocortical y para ayudar al radiólogo
intervencionista y al cirujano donde sea apropiado anatómicamente
Cuando el tratamiento quirúrgico es factible y
deseado por el paciente, el uso del muestreo venoso suprarrenal para hacer la
distinción entre enfermedad suprarrenal unilateral y bilateral
El uso de pruebas genéticas para el
hiperaldosteronismo familiar tipo 1 en pacientes en los que se confirma el
inicio del aldosteronismo primario antes de los 20 años y en aquellos con
antecedentes familiares de aldosteronismo primario o accidente cerebrovascular
a una edad temprana (<40 a="" o:p="" os="">
El uso de adrenalectomía laparoscópica unilateral en
pacientes con aldosteronismo primario unilateral documentado (es decir, adenoma
productor de aldosterona o hiperplasia suprarrenal unilateral) o, en pacientes
que no pueden o no desean someterse a cirugía, la administración de tratamiento
médico que incluye un antagonista del receptor mineralocorticoide
La administración de tratamiento médico con un
antagonista del receptor de mineralocorticoides en pacientes con aldosteronismo
primario debido a enfermedad suprarrenal bilateral
En pacientes con aldosteronismo remediable con
glucocorticoides, la administración de la dosis más baja de glucocorticoides
para reducir la hormona adrenocorticotrópica y así normalizar la presión
arterial y los niveles de potasio como tratamiento de primera línea; si la
presión sanguínea no se normaliza con el glucocorticoide solo, se puede agregar
un antagonista del receptor mineralocorticoide
RESUMEN DE MEDICACIÓN
En el aldosteronismo primario no quirúrgico, el
tratamiento médico es el tratamiento de elección. El fármaco que es el
tratamiento de primera elección para la mayoría de las variantes del
aldosteronismo primario no quirúrgico es la espironolactona, que se usa para
lograr el normoaldosteronismo y para ayudar con el control de la presión
arterial. Los suplementos de potasio no deben administrarse de forma rutinaria
con espironolactona debido a la posibilidad de desarrollar hipercalemia.
En pacientes que no pueden tolerar la
espironolactona, se pueden utilizar otros diuréticos ahorradores de potasio,
como la amilorida y el triamtereno, aunque se consideran opciones menos
ideales. [ 37 ]
El aldosteronismo remediable con glucocorticoides
(GRA) se trata con pequeñas dosis de glucocorticosteroides (es decir,
hidrocortisona, prednisona). En dosis óptimas, los glucocorticosteroides
normalizan la aldosterona y la presión arterial.
Se pueden agregar varios antihipertensivos para
lograr un control adecuado de la presión arterial. Los bloqueadores de los canales
de calcio dihidropiridínicos (p. Ej., Nifedipina) inhiben directamente la
producción de aldosterona; sin embargo, aunque producen mejorías significativas
en pacientes con hipertensión (HTA), no abordan la fisiopatología. La actividad
de la renina plasmática (PRA), los niveles de aldosterona, el volumen
plasmático y las concentraciones séricas de potasio permanecen esencialmente
sin cambios con el uso de nifedipina.
Otros agentes de segundo paso para el control de la
presión arterial incluyen los diuréticos tiazídicos, los inhibidores de la
enzima convertidora de la angiotensina (ECA) y los bloqueadores del receptor de
la angiotensina II. [ 23 ]
Una dieta restringida en sodio (menos de 80 mEq o
menos de2 g de sodio por día), el mantenimiento del peso corporal ideal y el
ejercicio aeróbico regular contribuyen sustancialmente al éxito del tratamiento
farmacológico.
ANTAGONISTAS DE ALDOSTERONA, SELECTIVOS
Estos agentes compiten con los sitios receptores de
aldosterona, reduciendo el edema y la ascitis.
ESPIRONOLACTONA (ALDACTONE)
La espironolactona se une competitivamente a los
receptores en el sitio de intercambio sodio-potasio dependiente de aldosterona en
el túbulo renal contorneado distal. Proporciona efectos diuréticos y
antihipertensivos, lo que provoca una mayor excreción de sodio y agua, al
tiempo que conserva el potasio. La espironolactona se administra sola o con un
agente diurético que actúa sobre el túbulo renal proximal. La espironolactona
puede bloquear los efectos de la aldosterona en los músculos lisos
arteriolares.
EPLERENONA (INSPRA)
La eplerenona bloquea selectivamente la aldosterona
en los receptores mineralocorticoides en los tejidos epiteliales (p. Ej.,
Riñones) y no epiteliales (p. Ej., Corazón, vasos sanguíneos, cerebro),
disminuyendo así la presión arterial y la reabsorción de sodio.
DIURÉTICOS AHORRADORES DE POTASIO
Estos agentes se usan como medicamentos de segunda
línea para el tratamiento del aldosteronismo primario debido a una enfermedad
no lateralizante y / o enfermedad de lateralización para la cual la cirugía
está contraindicada o rechazada. A menudo se deben usar con otros
antihipertensivos para lograr el mejor control de la presión arterial, ya que
no son antihipertensivos potentes.
TRIAMTERENE (DYRENIUM)
El triamtereno es un diurético ahorrador de potasio
con propiedades natriuréticas relativamente débiles. Ejerce un efecto diurético
en el túbulo renal distal para inhibir la reabsorción de sodio a cambio de
potasio e hidrógeno. El triamtereno aumenta la excreción de sodio y reduce la
pérdida excesiva de potasio e hidrógeno asociada con hidroclorotiazida. No es
un antagonista competitivo de mineralocorticoides; su efecto conservador de
potasio se observa en pacientes con enfermedad de Addison (es decir, sin
aldosterona).
El inicio y la duración de la actividad con
triamtereno son similares a los de hidroclorotiazida. No se demuestra un efecto
antihipertensivo predecible. Se absorbe rápidamente después de la
administración oral, y los niveles plasmáticos máximos se alcanzan dentro de 1
hora de la dosificación. El triamtereno se metaboliza principalmente a un
conjugado de sulfato de hidroxitriamtereno. Los niveles plasmáticos y urinarios
de este metabolito superan con creces los niveles de triamtereno.
AMILORIDA
Amilorida es una pirazina-carbonil-guanidina no
relacionada químicamente con otros agentes antiqualiuréticos o diuréticos
conocidos. Es un fármaco conservador del potasio (antiacaliurético) que, en
comparación con los diuréticos tiazídicos, posee actividad natriurética,
diurética y antihipertensiva débil. Los efectos de Amiloride han sido
parcialmente aditivos a los efectos de los diuréticos tiazídicos en algunos
estudios clínicos. Cuando se administra con una tiazida o diurético de asa, se
ha demostrado que disminuye la excreción urinaria aumentada de magnesio que
ocurre cuando se usa una tiazida o un diurético de asa solo.
La amilorida tiene actividad conservadora de potasio
en pacientes que reciben agentes diuréticos kaliuréticos. Amiloride no es un
antagonista de la aldosterona, y sus efectos se observan en ausencia de
aldosterona. Ejerce su efecto ahorrador de potasio a través de la inhibición de
la reabsorción de sodio en el túbulo contorneado distal, el túbulo colector
cortical y el conducto colector. Esto disminuye el potencial negativo neto de
la luz tubular y reduce la secreción de potasio e hidrógeno y sus excreciones
posteriores.
Amiloride por lo general comienza a actuar dentro de
las 2 horas después de una dosis oral. Su efecto sobre la excreción de
electrolitos alcanza un pico entre 6-10 horas y dura aproximadamente 24 horas.
Los niveles plasmáticos máximos se obtienen en 3-4 horas, y la vida media
plasmática del fármaco varía entre 6 y 9 horas.
Amiloride no es metabolizado por el hígado; en
cambio es excretado sin cambios por los riñones. Dentro de las 72 horas,
aproximadamente el 50% de una dosis de amilorida se excreta en la orina y el
40% en las heces. El medicamento tiene poco efecto sobre la tasa de filtración
glomerular o sobre el flujo sanguíneo renal. Debido a que el hígado no
metaboliza el hidrocloruro de amilorida, no se prevé la acumulación de
medicamentos en pacientes con disfunción hepática; sin embargo, la acumulación
puede ocurrir si se desarrolla el síndrome hepatorrenal.
Amiloride rara vez debe usarse solo. Usados como
agentes únicos, los diuréticos ahorradores de potasio, como la amilorida,
aumentan el riesgo de hipercalemia (aproximadamente 10% con amilorida).
Amiloride debe usarse solo solo cuando se haya documentado la hipocalemia
persistente y solo con una titulación cuidadosa de la dosis y una estrecha
monitorización de los niveles séricos de electrolitos.
DIURÉTICOS TIACÍDICOS
Los diuréticos tiazídicos inhiben la reabsorción de
sodio en los túbulos distales, aumentando la excreción de sodio, agua y iones
de potasio e hidrógeno. Han sido efectivos en el tratamiento de la hipertensión
de diversas etiologías. Además de disminuir la reabsorción de sodio, también
parecen disminuir la sensibilidad de los vasos sanguíneos a las sustancias
vasopresoras circulantes. En todos los pacientes tratados con diuréticos, se
deben controlar los niveles de electrolitos. Los ejemplos de diuréticos tiazídicos
son hidroclorotiazida y clortalidona.
HIDROCLOROTIAZIDA (MICROZIDE)
La hidroclorotiazida inhibe la reabsorción de sodio
en los túbulos distales, causando una mayor excreción de sodio y agua, así como
de iones de potasio e hidrógeno.
CLORTALIDONA
La clortalidona inhibe la reabsorción de sodio en
los túbulos distales, causando una mayor excreción de sodio y agua, así como de
iones de potasio e hidrógeno.
BLOQUEADORES DE LOS CANALES DE CALCIO
Los bloqueadores de los canales de calcio afectan la
presión arterial al disminuir la resistencia periférica vascular. Con los
bloqueadores de los canales de calcio de acción corta, la respuesta cardíaca a
esta acción es variable y puede producirse taquicardia. Las preparaciones de
acción prolongada pueden causar una disminución en la frecuencia cardíaca.
Los bloqueadores de los canales de calcio se
clasifican por su estructura y tienen diferentes grados de selectividad en sus
efectos sobre el músculo liso vascular. Las dihidropiridinas no ejercen efectos
electrofisiológicos y se usan comúnmente para controlar la hipertensión. Se
puede producir rubor facial. Los ejemplos de bloqueadores de los canales de
calcio incluyen amlodipina e isradipina.
AMLODIPINA (AMLOC)
La amlodipina se considera generalmente como una dihidropiridina,
aunque la evidencia experimental sugiere que también se puede unir a sitios de
unión a no dihidropiridina. Es apropiado para la profilaxis de la angina
variante y tiene efectos antianginosos y antihipertensivos. La amlodipina
bloquea la liberación postexcita de iones de calcio en el músculo liso vascular
y cardíaco, inhibiendo así la acción de la adenosina trifosfatasa (ATPasa) en
la contracción de miofibrillas.
El efecto global de la amlodipina es la reducción de
los niveles de calcio intracelular en las células cardíacas y de músculo liso
de la vasculatura coronaria y periférica, lo que da como resultado la
dilatación de las arterias coronarias y periféricas. La amlodipina también
aumenta el suministro de oxígeno al miocardio en pacientes con angina
vasoespástica y puede potenciar los efectos del inhibidor de la enzima
convertidora de la angiotensina (ECA).
Durante la despolarización, la amlodipina inhibe la
entrada de iones de calcio en canales lentos y áreas sensibles al voltaje del
músculo liso vascular y el miocardio. Beneficia a pacientes no embarazadas con
disfunción sistólica, hipertensión o arritmias. Tiene una vida media
sustancialmente más larga que nifedipina y diltiazem y se administra una vez al
día.
FELODIPINO
La felodipina relaja el músculo liso coronario y
produce vasodilatación coronaria, que a su vez mejora el suministro de oxígeno
al miocardio. Beneficia a pacientes no embarazadas con disfunción sistólica,
hipertensión o arritmias. Puede usarse durante el embarazo si está clínicamente
indicado.
Los bloqueadores de los canales de calcio potencian
los efectos del inhibidor de la ECA. La protección renal no está probada, pero
estos agentes reducen las tasas de morbilidad y mortalidad en la insuficiencia
cardíaca congestiva. Los bloqueadores de los canales de calcio están indicados
en pacientes con disfunción diastólica. Son efectivos como monoterapia en
pacientes negros y ancianos.
ISRADIPINA
Isradipina es un bloqueador de canales de calcio
dihidropiridina. Inhibe la entrada de calcio en áreas sensibles al voltaje
seleccionadas del músculo liso vascular y el miocardio durante la
despolarización. Esto causa la relajación del músculo liso vascular coronario,
lo que produce una vasodilatación coronaria. La vasodilatación reduce la
resistencia sistémica y la presión arterial, con un pequeño aumento en la
frecuencia cardíaca en reposo. Isradipina también tiene efectos inotrópicos
negativos.
NIFEDIPINA, DE LIBERACIÓN PROLONGADA (ADALAT CC,
NIFEDICAL XL, PROCARDIA XL)
La nifedipina de liberación prolongada relaja el
músculo liso coronario y produce vasodilatación coronaria, que a su vez mejora
el suministro de oxígeno al miocardio.
INHIBIDORES DE ECA
Los inhibidores de la enzima convertidora de la
angiotensina (ECA) previenen la conversión de angiotensina I a angiotensina II,
un potente vasoconstrictor y una menor secreción de aldosterona. Son fármacos
efectivos y bien tolerados sin efectos adversos sobre los niveles de lípidos en
plasma o la tolerancia a la glucosa. Impiden la progresión de la nefropatía
diabética y otras formas de glomerulopatías, pero parecen ser menos eficaces en
pacientes negros que en pacientes blancos. Los inhibidores de la ECA están
contraindicados en el embarazo.
Los pacientes con alta actividad de renina plasmática
(ARP) pueden tener una respuesta hipotensora excesiva a los inhibidores de la
ECA. Los pacientes con vasculopatía renal bilateral o con un solo riñón, cuya
perfusión renal se mantiene con altos niveles de angiotensina II, pueden
desarrollar insuficiencia renal aguda irreversible cuando se los trata con
inhibidores de la ECA, y se debe tener precaución con su uso en estos
pacientes. Curiosamente, aunque el aldosteronismo primario es una afección
asociada con baja renina plasmática, la secreción de aldosterona parece ser
exquisitamente sensible incluso a concentraciones subnormales de angiotensina
II. Este fenómeno parece ser la base de la eficacia de los inhibidores de la
ECA en el aldosteronismo primario (específicamente hiperplasia suprarrenal idiopática
[AHI]).
La tos y el angioedema son menos comunes con los
miembros más nuevos de esta clase que con el captopril. Deben controlarse las
concentraciones séricas de potasio y creatinina sérica para el desarrollo de
hipercalemia y azotemia. Los agentes en esta clase incluyen captopril,
lisinopril y enalapril.
CAPTOPRIL
El captopril previene la conversión de angiotensina
I a angiotensina II, un potente vasoconstrictor, lo que resulta en una menor
secreción de aldosterona. Se absorbe rápidamente, pero la biodisponibilidad se
reduce significativamente con la ingesta de alimentos. Captopril logra una
concentración máxima en 1 hora y tiene una vida media corta. La droga es
eliminada por el riñón; la función renal deteriorada requiere la reducción de
la dosis. Captopril se absorbe bien por vía oral.
Administre captopril al menos 1 hora antes de las
comidas. Si se agrega al agua, úselo en 15 minutos. La dosis puede ser baja al
principio, luego ajustarse según sea necesario y según lo tolere el paciente.
ENALAPRIL (VASOTEC)
Enalapril previene la conversión de angiotensina I a
angiotensina II, un potente vasoconstrictor, lo que resulta en niveles elevados
de renina plasmática y una reducción en la secreción de aldosterona. El
medicamento ayuda a controlar la presión sanguínea y la proteinuria. El
enalapril disminuye la relación de flujo pulmonar a sistémico en el laboratorio
de cateterización y aumenta el flujo sanguíneo sistémico en pacientes con
resistencia vascular pulmonar relativamente baja.
Enalapril tiene un efecto clínico favorable cuando
se administra durante un período prolongado. Debido a que ayuda a prevenir la
pérdida de potasio en los túbulos distales, el enalapril reduce la cantidad de
suplementos de potasio oral que necesita el paciente.
LISINOPRIL (PRINIVIL, ZESTRIL)
Lisinopril previene la conversión de angiotensina I
a angiotensina II, un vasoconstrictor potente, lo que resulta en niveles
elevados de renina en plasma y una reducción en la secreción de aldosterona.
BENAZEPRIL
Benazepril previene la conversión de angiotensina I
a angiotensina II, un vasoconstrictor potente, lo que resulta en niveles
elevados de renina plasmática y una reducción en la secreción de aldosterona.
Cuando los pacientes pediátricos no pueden tragar
las tabletas o la dosis calculada no se corresponde con la concentración de la
tableta, se puede combinar una suspensión extemporánea. Combine 300 mg (15
tabletas de 20 mg de concentración) en 75 ml de vehículo de suspensión Ora-Plus
y agite bien durante al menos 2 minutos. Deje que las tabletas se sientan y se
disuelvan durante al menos 1 hora, luego agite de nuevo durante 1 minuto.
Agregue 75 ml de Ora-Sweet. La concentración final es de 2 mg / ml, con un
volumen total de 150 ml. El tiempo de caducidad es de 30 días con refrigeración.
FOSINOPRIL
Fosinopril es un inhibidor de la ECA competitivo.
Previene la conversión de angiotensina I a angiotensina II, un potente
vasoconstrictor, lo que resulta en niveles elevados de renina en plasma y una
reducción en la secreción de aldosterona. Disminuye la presión intraglomerular
y la filtración de proteína glomerular al disminuir la constricción arteriolar
eferente.
QUINAPRIL
Quinapril es un inhibidor de la ECA competitivo.
Reduce los niveles de angiotensina II, disminuyendo la secreción de
aldosterona.
RAMIPRIL (TRITACE)
Ramipril inhibe inhibe parcialmente tanto la
actividad de la ECA circulante como del tejido, por lo tanto, reduce la
formación de angiotensina II en el tejido y el plasma. Ramipril tiene un efecto
antihipertensivo incluso en pacientes con hipertensión de baja renina.
BLOQUEADORES DEL RECEPTOR DE ANGIOTENSINA II
Los bloqueadores de los receptores de la
angiotensina II reducen la presión sanguínea al bloquear el receptor final (es
decir, la angiotensina II) en el eje renina-angiotensina. Al igual que los
inhibidores de la enzima convertidora de la angiotensina (ECA), están
contraindicados en el embarazo. Deben controlarse los niveles séricos de
electrolitos y creatinina. Irbesartan y losartán son ejemplos de bloqueadores del
receptor de angiotensina II (BRA). Curiosamente, aunque el aldosteronismo
primario es una afección asociada con baja renina plasmática, la secreción de
aldosterona parece ser exquisitamente sensible incluso a concentraciones
subnormales de angiotensina II. Este fenómeno parece ser la base de la eficacia
de los BRA en aldosteronismo primario (específicamente hiperplasia suprarrenal
idiopática [AHI]).
IRBESARTAN (AVAPRO)
Irbesartan bloquea los efectos vasoconstrictores y
secretores de aldosterona de la angiotensina II en el sitio del receptor del
tejido. Puede inducir una inhibición más completa del sistema
renina-angiotensina que los inhibidores de la ECA. Además, irbesartan no afecta
la respuesta a la bradiquinina, y es menos probable que se asocie con tos y
angioedema.
LOSARTAN (COZAAR)
Losartan bloquea los efectos vasoconstrictores y
secretores de aldosterona de la angiotensina II. Puede inducir una inhibición
más completa del sistema renina-angiotensina que los inhibidores de la ECA.
Además, losartan no afecta la respuesta a la bradiquinina, y es menos probable
que se asocie con tos y angioedema. Es adecuado para pacientes que no pueden
tolerar los inhibidores de la ECA.
OLMESARTAN
Olmesartan bloquea los efectos vasoconstrictores de
la angiotensina II al bloquear selectivamente la unión de la angiotensina II a
los receptores de la angiotensina II tipo 1 en el músculo liso vascular. Su
acción es independiente de las vías para la síntesis de angiotensina II.
VALSARTAN (DIOVAN)
Valsartan es un profármaco que desplaza la
angiotensina II de los receptores de angiotensina II tipo 1, bloqueando los
efectos vasoconstrictores de la angiotensina II. Valsartan también puede
disminuir la presión arterial a través de sus efectos sobre la liberación de
aldosterona, la liberación de catecolaminas, la liberación de arginina
vasopresina, la ingesta de agua y las respuestas hipertróficas.
Valsartan puede inducir una inhibición más completa
del sistema renina-angiotensina que los inhibidores de la ECA. Además, no
afecta la respuesta a la bradiquinina y es menos probable que se asocie con tos
y angioedema. Valsartan es adecuado para pacientes que no pueden tolerar los
inhibidores de la ECA.
TELMISARTAN (MICARDIS)
Telmisartan bloquea el vasoconstrictor y los efectos
secretores de aldosterona de la angiotensina II al bloquear selectivamente la
unión de la angiotensina II al receptor AT1 en muchos tejidos, como el músculo
liso vascular y la glándula suprarrenal y, por lo tanto, reduce la presión
arterial. También se encuentra un receptor AT2 en muchos tejidos, pero se
desconoce si AT2 está asociado con la homeostasis cardiovascular y telmisartan
tiene una afinidad mucho mayor por el receptor AT1 que por el receptor AT2.
CORTICOSTEROIDES
Esta clase de agentes son terapéuticamente
apropiados solo para el subtipo GRA de aldosteronismo primario. El tratamiento
de elección en GRA es la administración de la dosis más baja posible de
glucocorticoides que se puede usar para lograr un control adecuado de la
presión arterial. Debido a los posibles efectos adversos que pueden resultar
incluso de un exceso sutil de glucocorticoides, el uso de glucocorticoides de
acción corta, como la prednisona y la hidrocortisona (en lugar de la
dexametasona), generalmente es lo mejor.
PREDNISONA
La prednisona es un profármaco de acción corta que
ejerce sus efectos después de que se metaboliza y se convierte en prednisolona.
La prednisona imita el cortisol de origen natural y se usa en GRA para suprimir
rápidamente los niveles de aldosterona y resolver la expansión del volumen y la
hipertensión en este trastorno, siendo generalmente eficaz en las 2 semanas
posteriores al inicio del tratamiento.
HIDROCORTISONA
La hidrocortisona posee una similitud molecular con
la aldosterona y, por lo tanto, no solo se une al receptor de glucocorticoides
(resultando en menores niveles de aldosterona en la GRA), sino también al
receptor mineralocorticoide (MR), lo que también proporciona una inhibición
competitiva de los niveles ambientales de aldosterona en la MR nivel (que
resulta en la disminución de los efectos fisiológicos de los niveles
ambientales existentes de aldosterona en GRA).
Rossi GP, Ragazzo F, Seccia TM, Maniero C, Barisa M,
Calò LA, et al. Hyperparathyroidism
can be useful in the identification of primary aldosteronism due to
aldosterone-producing adenoma. Hypertension. 2012 Aug. 60(2):431-6. [Medline].
Dluhy RG, Lifton
RP. Glucocorticoid-remediable aldosteronism. Endocrinol Metab Clin North Am.
1994 Jun. 23(2):285-97. [Medline].
Funder JW. The
genetic basis of primary aldosteronism. Curr Hypertens Rep. 2012 Apr.
14(2):120-4. [Medline].
Choi M, Scholl
UI, Yue P, et al. K+ channel mutations in adrenal aldosterone-producing
adenomas and hereditary hypertension. Science. 2011 Feb 11. 331(6018):768-72.
[Medline]. [Full Text].
Young DB.
Quantitative analysis of aldosterone's role in potassium regulation. Am J
Physiol. 1988 Nov. 255(5 Pt 2):F811-22. [Medline].
Stowasser M,
Klemm SA, Tunny TJ, et al. Plasma aldosterone response to ACTH in subtypes of
primary aldosteronism. Clin Exp Pharmacol Physiol. 1995 Jun-Jul. 22(6-7):460-2.
[Medline].
Litchfield WR,
New MI, Coolidge C, et al. Evaluation of the dexamethasone suppression test for
the diagnosis of glucocorticoid-remediable aldosteronism. J Clin Endocrinol
Metab. 1997 Nov. 82(11):3570-3. [Medline]. [Full Text].
Mulatero P,
Stowasser M, Loh KC, Fardella CE, Gordon RD, Mosso L, et al. Increased
diagnosis of primary aldosteronism, including surgically correctable forms, in
centers from five continents. J Clin Endocrinol Metab. 2004 Mar. 89(3):1045-50.
[Medline].
Born-Frontsberg
E, Reincke M, Rump LC, et al. Cardiovascular and cerebrovascular comorbidities
of hypokalemic and normokalemic primary aldosteronism: results of the German
Conn's Registry. J Clin Endocrinol Metab. 2009 Apr. 94(4):1125-30. [Medline].
Bernini G,
Galetta F, Franzoni F, Bardini M, Taurino C, Bernardini M, et al. Arterial
stiffness, intima-media thickness and carotid artery fibrosis in patients with
primary aldosteronism. J Hypertens. 2008 Dec. 26(12):2399-405. [Medline].
Apostolopoulou
K, Künzel HE, Gerum S, Merkle K, Schulz S, Fischer E, et al. Gender differences
in anxiety and depressive symptoms in patients with primary hyperaldosteronism:
A cross-sectional study. World J Biol Psychiatry. 2012 May 8. [Medline].
Cruz DN,
Perazella MA. Hypertension and hypokalemia: unusual syndromes. Conn Med. 1997
Feb. 61(2):67-75. [Medline].
Cesari M,
Letizia C, Angeli P, Sciomer S, Rosi S, Rossi GP. Cardiac Remodeling in
Patients With Primary and Secondary Aldosteronism: A Tissue Doppler Study. Circ
Cardiovasc Imaging. 2016 Jun. 9 (6):[Medline].
Hall JE, Granger
JP, Smith MJ Jr. Role of renal hemodynamics and arterial pressure in
aldosterone "escape". Hypertension. 1984.
6:1183.
Yokota N, Bruneau BG, Kuroski de Bold ML, et al. Atrial natriuretic factor significantly contributes to
the mineralocorticoid escape phenomenon. Evidence for a guanylate
cyclase-mediated pathway. J Clin Invest. 1994 Nov. 94(5):1938-46. [Medline].
[Full Text].
Vallon V, Rieg
T. Regulation of renal NaCl and water transport by the ATP/UTP/P2Y2 receptor
system. Am J Physiol Renal Physiol. 2011 Sep. 301(3):F463-75. [Medline]. [Full
Text].
Schiffrin EL,
Chrétien M, Seidah NG, et al. Response of human aldosteronoma cells in culture
to the N-terminal glycopeptide of pro-opiomelanocortin and gamma 3-MSH. Horm
Metab Res. 1983 Apr. 15(4):181-4. [Medline].
[Guideline]
Funder JW, Carey RM, Fardella C, Gomez-Sanchez CE, Mantero F, Stowasser M, et
al. Case detection, diagnosis, and treatment of patients with primary
aldosteronism: an endocrine society clinical practice guideline. J Clin
Endocrinol Metab. 2008 Sep. 93(9):3266-81. [Medline].
Quamme GA.
Control of magnesium transport in the thick ascending limb. Am J Physiol. 1989
Feb. 256(2 Pt 2):F197-210. [Medline].
Seiler L, Rump
LC, Schulte-Mönting J, Slawik M, Borm K, Pavenstädt H, et al. Diagnosis of
primary aldosteronism: value of different screening parameters and influence of
antihypertensive medication. Eur J Endocrinol. 2004 Mar.
150(3):329-37. [Medline].
Tzanela M, Effremidis G, Vassiliadi D, et al. The aldosterone to renin ratio in the evaluation of
patients with incidentally detected adrenal masses. Endocrine. 2007 Oct.
32(2):136-42. [Medline].
Diederich S, Mai
K, Bahr V, et al. The simultaneous measurement of plasma-aldosterone- and
-renin-concentration allows rapid classification of all disorders of the
renin-aldosterone system. Exp Clin Endocrinol Diabetes. 2007 Jul. 115(7):433-8.
[Medline].
Wu VC, Chang HW,
Liu KL, et al. Primary aldosteronism: diagnostic accuracy of the losartan and
captopril tests. Am J Hypertens. 2009 Aug. 22(8):821-7. [Medline].
Burton TJ,
Mackenzie IS, Balan K, Koo B, Bird N, Soloviev DV, et al. Evaluation of the
sensitivity and specificity of (11)C-metomidate positron emission tomography
(PET)-CT for lateralizing aldosterone secretion by Conn's adenomas. J Clin
Endocrinol Metab. 2012 Jan. 97(1):100-9. [Medline].
Otsuka F,
Otsuka-Misunaga F, Koyama S, et al. Hormonal characteristics of primary aldosteronism
due to unilateral adrenal hyperplasia. J Endocrinol Invest. 1998 Sep.
21(8):531-6. [Medline].
Stowasser M,
Bachmann AW, Tunny TJ. Production of 18-oxo-cortisol in subtypes of primary
aldosteronism. Clin Exp Pharmacol Physiol. 1996 Jun-Jul. 23(6-7):591-3.
[Medline].
Hamlet SM,
Gordon RD, Gomez-Sanchez CE, et al. Adrenal transitional zone steroids, 18-oxo
and 18-hydroxycortisol, useful in the diagnosis of primary aldosteronism, are
ACTH-dependent. Clin Exp Pharmacol Physiol. 1988 Apr. 15(4):317-22. [Medline].
McAlister FA,
Lewanczuk RZ. Primary hyperaldosteronism and adrenal incidentaloma: an argument
for physiologic testing before adrenalectomy. Can J Surg. 1998 Aug.
41(4):299-305. [Medline].
Di Martino M,
Garcia Sanz I, Munoz de Nova JL, Marin Campos C, Martinez Martin M, Dominguez
Gadea L. NP-59 test for preoperative localization of primary
hyperaldosteronism. Langenbecks Arch Surg. 2017 Feb 21. [Medline].
Georgiades CS,
Hong K, Geschwind JF, et al. Adjunctive use of C-arm CT may eliminate technical
failure in adrenal vein sampling. J Vasc Interv Radiol. 2007 Sep. 18(9):1102-5.
[Medline].
Young WF,
Stanson AW, Grant CS, et al. Primary aldosteronism: adrenal venous sampling.
Surgery. 1996 Dec. 120(6):913-9; discussion 919-20. [Medline].
Webb R, Mathur
A, Chang R, Baid S, Nilubol N, Libutti SK, et al. What is the Best Criterion
for the Interpretation of Adrenal Vein Sample Results in Patients with Primary
Hyperaldosteronism?. Ann Surg Oncol. 2011 Nov 3. [Medline].
Dekkers T,
Prejbisz A, Kool LJ, et al. Adrenal vein sampling versus CT scan to determine
treatment in primary aldosteronism: an outcome-based randomised diagnostic
trial. Lancet Diabetes Endocrinol. 2016 Sep. 4 (9):739-46. [Medline].
Young WF,
Stanson AW, Thompson GB, et al. Role for adrenal venous sampling in primary
aldosteronism. Surgery. 2004 Dec. 136(6):1227-35. [Medline].
Naruse M, Naruse
K, Yoshimoto T, et al. Dopaminergic regulation of aldosterone secretion: its
pathophysiologic significance in subsets of primary aldosteronism. Hypertens
Res. 1995 Jun. 18 Suppl 1:S59-64. [Medline].
Carey RM.
Primary aldosteronism. Horm Res. 2009 Jan. 71 Suppl 1:8-12. [Medline].
Hood SJ, Taylor
KP, Ashby MJ, et al. The spironolactone, amiloride, losartan, and thiazide
(SALT) double-blind crossover trial in patients with low-renin hypertension and
elevated aldosterone-renin ratio. Circulation. 2007 Jul 17. 116(3):268-75.
[Medline]. [Full Text].
Ronconi V,
Turchi F, Appolloni G, di Tizio V, Boscaro M, Giacchetti G. Aldosterone,
Mineralocorticoid Receptor and the Metabolic Syndrome: Role of the
Mineralocorticoid Receptor Antagonists. Curr Vasc Pharmacol. 2011 Oct 21.
[Medline].
Minowada S,
Fujimura T, Takahashi N, et al. Computed tomography-guided percutaneous acetic
acid injection therapy for functioning adrenocortical adenoma. J Clin
Endocrinol Metab. 2003 Dec. 88(12):5814-7. [Medline]. [Full Text].
Sukor N, Gordon
RD, Ku YK, et al. Role of unilateral adrenalectomy in bilateral primary
aldosteronism: a 22-year single center experience. J Clin Endocrinol Metab.
2009 Jul. 94(7):2437-45. [Medline].
Celen O, O'Brien
MJ, Melby JC, et al. Factors influencing outcome of surgery for primary
aldosteronism. Arch Surg. 1996 Jun. 131(6):646-50. [Medline].
Waldmann J,
Maurer L, Holler J, Kann PH, Ramaswamy A, Bartsch DK, et al. Outcome of surgery
for primary hyperaldosteronism. World J Surg. 2011 Nov. 35(11):2422-7.
[Medline].
Letavernier E,
Peyrard S, Amar L, et al. Blood pressure outcome of adrenalectomy in patients
with primary hyperaldosteronism with or without unilateral adenoma. J
Hypertens. 2008 Sep. 26(9):1816-23. [Medline].
Milsom SR,
Espiner EA, Nicholls MG, et al. The blood pressure response to unilateral
adrenalectomy in primary aldosteronism. Q J Med. 1986 Dec. 61(236):1141-51.
[Medline].
Giacchetti G,
Turchi F, Boscaro M, Ronconi V. Management of primary aldosteronism: its
complications and their outcomes after treatment. Curr Vasc Pharmacol. 2009
Apr. 7(2):244-49. [Medline].
Amar L, Baguet
JP, Bardet S, et al. SFE/SFHTA/AFCE primary aldosteronism consensus:
Introduction and handbook. Ann Endocrinol (Paris). 2016 Jun 14. [Medline].
[Full Text].
Baguet JP,
Steichen O, Mounier-Vehier C, Gosse P. SFE/SFHTA/AFCE consensus on primary
aldosteronism, part 1: Epidemiology of PA, who should be screened for sporadic
PA?. Ann Endocrinol (Paris). 2016 Apr 15. 86 (20):1002-8. [Medline]. [Full
Text].
Douillard C,
Houillier P, Nussberger J, Girerd X. SFE/SFHTA/AFCE Consensus on Primary
Aldosteronism, part 2: First diagnostic steps. Ann Endocrinol (Paris). 2016 May
10. [Medline]. [Full Text].
Reznik Y, Amar
L, Tabarin A. SFE/SFHTA/AFCE consensus on primary aldosteronism, part 3:
Confirmatory testing. Ann Endocrinol (Paris). 2016 Jun 15. [Medline]. [Full
Text].
Bardet S,
Chamontin B, Douillard C, et al. SFE/SFHTA/AFCE consensus on primary
aldosteronism, part 4: Subtype diagnosis. Ann Endocrinol (Paris). 2016 Mar 29.
[Medline]. [Full Text].
Zennaro MC,
Jeunemaitre X. SFE/SFHTA/AFCE consensus on primary aldosteronism, part 5:
Genetic diagnosis of primary aldosteronism. Ann Endocrinol (Paris). 2016 Jun
14. [Medline]. [Full Text].
Steichen O, Amar
L, Chaffanjon P, Kraimps JL, Menegaux F, Zinzindohoue F. SFE/SFHTA/AFCE
consensus on primary aldosteronism, part 6: Adrenal surgery. Ann Endocrinol
(Paris). 2016 Jun 10. [Medline]. [Full Text].
Pechère-Bertschi
A, Herpin D, Lefebvre H. SFE/SFHTA/AFCE consensus on primary aldosteronism,
part 7: Medical treatment of primary aldosteronism. Ann Endocrinol (Paris).
2016 Jun 14. [Medline]. [Full Text].
[Guideline]
Funder JW, Carey RM, Mantero F, et al. The Management of Primary Aldosteronism:
Case Detection, Diagnosis, and Treatment: An Endocrine Society Clinical
Practice Guideline. J Clin Endocrinol Metab. 2016 May. 101 (5):1889-916.
[Medline]. [Full Text].
[Guideline] Romero
DG, Yanes Cardozo LL. Clinical Practice Guideline for Management of Primary
Aldosteronism: What is New in the 2016 Update?. Int J Endocrinol Metab Disord.
2016. 2 (3):[Medline]. [Full Text].