Introducción:
Las infecciones de partes blandas pueden ocurrir después de exposición a agua dulce o a agua salada, especialmente si esta se asocia a trauma. El trauma puede ser causado por criaturas vivas, u objetos inanimados encontrados en un medio acuático. Además algunas especies animales acuáticas pueden transmitir infecciones de partes blandas, fuera de un ambiente acuático. Esto puede ocurrir por ejemplo, con el uso de sanguijuelas con fines médicos, como se hace para aliviar la congestión venosa en sitios quirúrgicos. En estos casos, Aeromona sp, un habitante normal del intestino de las sanguijuelas puede ser la causa de la infección.
Aunque la variedad de microorganismos que pueden producir infección de partes blandas siguiendo a la exposición al agua es extremadamente amplia, esta revisión enfocará las cinco bacterias que más comúnmente producen este tipo de infeciones. Ellas son Aeromonas s/p, Edwardsiella tarda, Erysipelothrix rhusiopathiae, Vibrio vulnificus, y Mycobacterium marinum.
Las infecciones de partes blandas pueden ocurrir después de exposición a agua dulce o a agua salada, especialmente si esta se asocia a trauma. El trauma puede ser causado por criaturas vivas, u objetos inanimados encontrados en un medio acuático. Además algunas especies animales acuáticas pueden transmitir infecciones de partes blandas, fuera de un ambiente acuático. Esto puede ocurrir por ejemplo, con el uso de sanguijuelas con fines médicos, como se hace para aliviar la congestión venosa en sitios quirúrgicos. En estos casos, Aeromona sp, un habitante normal del intestino de las sanguijuelas puede ser la causa de la infección.
Aunque la variedad de microorganismos que pueden producir infección de partes blandas siguiendo a la exposición al agua es extremadamente amplia, esta revisión enfocará las cinco bacterias que más comúnmente producen este tipo de infeciones. Ellas son Aeromonas s/p, Edwardsiella tarda, Erysipelothrix rhusiopathiae, Vibrio vulnificus, y Mycobacterium marinum.
El acrónimo AEEVM será usado para mencionar dichos agentes en su conjunto.
Epidemiología.
El trauma o la injuria local, que puede ser menor o mayor, asociado a la exposición al agua es el fenómeno común que predispone a muchas de las infecciones relacionadas a AEEVM.
Trauma:
El trauma que lleva a infección con AEEVM incluye las heridas punzantes debidas a anzuelos o espinas de pescados, y laceraciones debidas a aletas de motores de propulsión de botes, así como una gran variedad de heridas producidas por objetos inanimados presentes en áreas acuáticas. Además del trauma por objetos inanimados, las mordeduras de peces, caimanes, cocodrilos, tiburones y tortugas pueden transmitir infecciones por AEEVM.
Epidemiología.
El trauma o la injuria local, que puede ser menor o mayor, asociado a la exposición al agua es el fenómeno común que predispone a muchas de las infecciones relacionadas a AEEVM.
Trauma:
El trauma que lleva a infección con AEEVM incluye las heridas punzantes debidas a anzuelos o espinas de pescados, y laceraciones debidas a aletas de motores de propulsión de botes, así como una gran variedad de heridas producidas por objetos inanimados presentes en áreas acuáticas. Además del trauma por objetos inanimados, las mordeduras de peces, caimanes, cocodrilos, tiburones y tortugas pueden transmitir infecciones por AEEVM.
Exposición al Agua:
Una variedad de tipos de exposición al agua puede ocasionar infecciones debidas a AEEVM. Estas incluyen agua dulce, agua salada, agua salitrosa, agua en piscinas y acuarios. M marinum está más relacionado con exposición a peceras, acuarios o piscinas, mientras que Vibrio vulnificus está limitado a exposición a agua salada o salitrosa.
Hubo un brote de infección de heridas por Aeromona. hidrophila reportado en 2004 en Australia con una tasa de ataque de 40% después de un partido de football en el barro. El microorganismo se aisló de una muestra de agua de un río utilizada para irrigar el campo de juego previo al partido, y se teorizó que abrasiones de piel pueden haber sido la puerta de entrada entre los afectados.
E. tarda es un microorganismo infrecuente como patógeno en el humano, que causa predominantemente enfermedad gastrointestinal. Sin embargo, las infecciones de heridas, incluyendo mionecrosis han ocurrido cuando las heridas son expuestas a un medio ambiente marino.
Predilección por Sexo:
Se ha visto que 90% de las infecciones por Aeromonas y Vibrio sp extraintestinales se ven en hombres, probablemente relacionadas con la mayor exposición de actividades al aire libre en el sexo masculino. También, el menor contenido de hierro en la mujer respecto del hombre la protegería contra infecciones con V vulnificus tal como se verá.
Enfermedades de Base:
Los pacientes con enfermedades hepáticas de base o cáncer tienen un riesgo aumentado de infecciones por AEEVM y pueden presentarse como una infección que pone en riesgo la vida del paciente. Esos pacientes están en particular riesgo de infección debido a Aeromonas sp, V. vulnificus, y E. tarda. La enfermedad diseminada desde un foco de infección de partes blandas es común en pacientes inmunocomprometidos.
Manifestaciones Clínicas
AEEVM pueden producir una variedad de infecciones de partes blandas incluyendo celulitis, formación de abscesos, infección de heridas, ectima gangrenoso, y procesos necrotizantes de partes blandas (por ej fascitis y miositis). Es difícil determinar la etiología de una infección basado solamente en elementos clínicos, ya que otros organismos como estreptococo beta hemolítico o stafilococo aureus pueden dar manifestaciones similares.
La presentación clínica y la severidad de la enfermedad puede ser extremadamente variable, y esto está relacionado en parte a la condición inmunológica y el estado de enfermedad de base del paciente o enfermedad hepática vista en algunos pacientes con riesgo de presentar infecciones por AEEVM.
La infección de partes blandas rápidamente progresiva con fiebre, y en pacientes de alto riesgo, puede haber sepsis por Aeromonas sp e infección por V. vulnificus. Una consideración especial debe hacerse para V. vulnificus como agente etiológico en un paciente con infección agresiva de partes blandas (por ejemplo celulitis bullosa) y necrosis de tejidos blandos (Figura A)

Figura A. Lesiones bullosas de piel vistas en 75% de los pacientes con infecciones por Vibrio. vulnificus
En contraste, las infecciones de partes blandas debidas a M. marinum y E. rhusiopathiae son generalmente indolentes y no están asociadas a toxicidad sistémica.
Las lesiones por M. marinum usualmente aparecen en una extremidad, especialmente en los codos, rodillas, y dorso de pies y manos, progresando subsecuentemente a ulceraciones superficiales y formación de cicatrices. La mayoría de las lesiones son solitarias, aunque ocasionalmente producen la “diseminación esporotricoidea” ascendentes que recuerdan la esporotricosis, que es también llamada linfangitis nodular. El compromiso de los ganglios regionales es infrecuente.

Una variedad de tipos de exposición al agua puede ocasionar infecciones debidas a AEEVM. Estas incluyen agua dulce, agua salada, agua salitrosa, agua en piscinas y acuarios. M marinum está más relacionado con exposición a peceras, acuarios o piscinas, mientras que Vibrio vulnificus está limitado a exposición a agua salada o salitrosa.
Hubo un brote de infección de heridas por Aeromona. hidrophila reportado en 2004 en Australia con una tasa de ataque de 40% después de un partido de football en el barro. El microorganismo se aisló de una muestra de agua de un río utilizada para irrigar el campo de juego previo al partido, y se teorizó que abrasiones de piel pueden haber sido la puerta de entrada entre los afectados.
E. tarda es un microorganismo infrecuente como patógeno en el humano, que causa predominantemente enfermedad gastrointestinal. Sin embargo, las infecciones de heridas, incluyendo mionecrosis han ocurrido cuando las heridas son expuestas a un medio ambiente marino.
Predilección por Sexo:
Se ha visto que 90% de las infecciones por Aeromonas y Vibrio sp extraintestinales se ven en hombres, probablemente relacionadas con la mayor exposición de actividades al aire libre en el sexo masculino. También, el menor contenido de hierro en la mujer respecto del hombre la protegería contra infecciones con V vulnificus tal como se verá.
Enfermedades de Base:
Los pacientes con enfermedades hepáticas de base o cáncer tienen un riesgo aumentado de infecciones por AEEVM y pueden presentarse como una infección que pone en riesgo la vida del paciente. Esos pacientes están en particular riesgo de infección debido a Aeromonas sp, V. vulnificus, y E. tarda. La enfermedad diseminada desde un foco de infección de partes blandas es común en pacientes inmunocomprometidos.
Manifestaciones Clínicas
AEEVM pueden producir una variedad de infecciones de partes blandas incluyendo celulitis, formación de abscesos, infección de heridas, ectima gangrenoso, y procesos necrotizantes de partes blandas (por ej fascitis y miositis). Es difícil determinar la etiología de una infección basado solamente en elementos clínicos, ya que otros organismos como estreptococo beta hemolítico o stafilococo aureus pueden dar manifestaciones similares.
La presentación clínica y la severidad de la enfermedad puede ser extremadamente variable, y esto está relacionado en parte a la condición inmunológica y el estado de enfermedad de base del paciente o enfermedad hepática vista en algunos pacientes con riesgo de presentar infecciones por AEEVM.
La infección de partes blandas rápidamente progresiva con fiebre, y en pacientes de alto riesgo, puede haber sepsis por Aeromonas sp e infección por V. vulnificus. Una consideración especial debe hacerse para V. vulnificus como agente etiológico en un paciente con infección agresiva de partes blandas (por ejemplo celulitis bullosa) y necrosis de tejidos blandos (Figura A)

Figura A. Lesiones bullosas de piel vistas en 75% de los pacientes con infecciones por Vibrio. vulnificus
En contraste, las infecciones de partes blandas debidas a M. marinum y E. rhusiopathiae son generalmente indolentes y no están asociadas a toxicidad sistémica.
Las lesiones por M. marinum usualmente aparecen en una extremidad, especialmente en los codos, rodillas, y dorso de pies y manos, progresando subsecuentemente a ulceraciones superficiales y formación de cicatrices. La mayoría de las lesiones son solitarias, aunque ocasionalmente producen la “diseminación esporotricoidea” ascendentes que recuerdan la esporotricosis, que es también llamada linfangitis nodular. El compromiso de los ganglios regionales es infrecuente.

(Figura 2). Granuloma de la Pecera.
Nódulos debidos a Mycobacterium marinum en un hombre diabético que desarrolló después de varias semanas de haber limpiado una pecera sin guantes y con una herida cortante en su dedo índice.
Nódulos debidos a Mycobacterium marinum en un hombre diabético que desarrolló después de varias semanas de haber limpiado una pecera sin guantes y con una herida cortante en su dedo índice.
E.rhusiopathiae más comúnmente causa una erupción cutánea localizada, erisipeloide, en los dedos de las manos de los pescadores o los empaquetadores de mariscos, cuando sufren traumas menores mientras manejan bivalvos contaminados, cangrejos, o pescados.
E. tarda causa infección de partes blandas inusualmente, aunque ha estado asociada con un espectro de manifestaciones desde una celulitis simple, similar a la celulitis debida a S.aureus y estreptococo beta hemolítico, hasta una infección fulminante de una herida complicada por bacteriemia, en pacientes con enfermedades hepáticas de base.
Infecciones por Aeromonas
Introducción:
E. tarda causa infección de partes blandas inusualmente, aunque ha estado asociada con un espectro de manifestaciones desde una celulitis simple, similar a la celulitis debida a S.aureus y estreptococo beta hemolítico, hasta una infección fulminante de una herida complicada por bacteriemia, en pacientes con enfermedades hepáticas de base.
Infecciones por Aeromonas
Introducción:
El género Aeromonas consiste en un bacilo gram negativo ubicuo, ampliamente distribuido en el agua dulce, aguas estuarinas, y ambientes marinos en todo el mundo. Las especies de Aeromonas crecen en un amplio rango de temperaturas, pero son aislados con mayor frecuencia los meses más cálidos. Por más de 100 años, las aeromonas han sido reconocidas como la causa de un amplio espectro de enfermedades entre los animales de sangre caliente, y también peces, reptiles, anfibios, mamíferos y humanos.
Microbiología:
El género Aeromonas fue parte de la familia Vibrionaceae hasta mediados de la década de 1980, momento en el que las evidencias filogenéticas derivadas de estudios moleculares las ubicaron en la familia Aeromonadaceae.
Las especies de Aeromonas son oxidasa positivas y fermentan la glucosa. Los organismos crecen en un rango térmico de 0º a 42ºC.
El género Aeromonas fue parte de la familia Vibrionaceae hasta mediados de la década de 1980, momento en el que las evidencias filogenéticas derivadas de estudios moleculares las ubicaron en la familia Aeromonadaceae.
Las especies de Aeromonas son oxidasa positivas y fermentan la glucosa. Los organismos crecen en un rango térmico de 0º a 42ºC.
Patogénesis:
La virulencia de las especies de Aeromonas es multifactorial. Los posibles factores de virulencia incluyen toxinas (citotóxicas y citotónicas), proteasas, hemolisinas, lipasas, adhesinas, aglutininas, pili, enterotoxinas, varias enzimas, y cubiertas de membranas, tales como capa-S y cápsula. Otros factores que pueden contribuir a la virulencia incluyen VacB, enolasa, y la presencia de un sistema de secreción Tipo VI.
Epidemiología:
Los reservorios ambientales son:
• Agua dulce.
• Agua de estuarios (agua salitrosa).
• Agua de superficie, especialmente recreacionales.
• Agua embotellada para tomar, incluyendo el agua tratada.
• Agua de zonas pantanosas y barro.
Las Aeromonas no son consideradas organismos marinos, pero pueden ser encontrados naturalmente en sistemas marinos en su interfase con el agua dulce (estuarios, desembocaduras de ríos en el mar). Sobreviven incluso a altas concentraciones de sal. Usualmente no son parte de la población bacteriana autóctona del agua subterránea, que normalmente es pobre en nutrientes. Sin embargo, Aeromonas sp pueden desarrollar en agua rica en un gran número de nutrientes, alcanzando un pico los meses de verano, tanto en lagos de agua dulce como aguas cloradas para beber. Mientras no sea considerada de origen fecal, estos organismos son tolerados como polutantes. La presencia de Aeromonas sp en alimentos refleja más probablemente el contacto de esos alimentos con agua, como es reflejado por el nombre de especies de tipo A. hydrofila, que significa “que ama el agua”.
Las infecciones humanas eran consideradas oportunistas, solo capaces de infectar individuos inmunocomprometidos. Sin embargo ahora se acepta que pueden causar un amplio rango de enfermedades extraintestinales en inmunocompetentes.
Hay controversia en cuanto al rol de Aeromonas en diarrea y enfermedad gastrointestinal; el aislamiento de Aeromonas en muchos pacientes asintomáticos ha sido problemático en cuanto a asignarle un rol, pero también se la ha aislado en pacientes con diarrea, de manera análoga a la Escherichia coli, por lo tanto la interpretación debe contextualizarse en la clínica y el laboratorio de un paciente determinado.
Manifestaciones Clínicas:
Aunque la enfermedad diarreica es probablemente la manifestación más común de infección por Aeromons, el organismo ha estado asociado a una variedad de presentaciones clínicas que van desde la infección de heridas hasta la bacteriemia.
Diarrea:
La virulencia de las especies de Aeromonas es multifactorial. Los posibles factores de virulencia incluyen toxinas (citotóxicas y citotónicas), proteasas, hemolisinas, lipasas, adhesinas, aglutininas, pili, enterotoxinas, varias enzimas, y cubiertas de membranas, tales como capa-S y cápsula. Otros factores que pueden contribuir a la virulencia incluyen VacB, enolasa, y la presencia de un sistema de secreción Tipo VI.
Epidemiología:
Los reservorios ambientales son:
• Agua dulce.
• Agua de estuarios (agua salitrosa).
• Agua de superficie, especialmente recreacionales.
• Agua embotellada para tomar, incluyendo el agua tratada.
• Agua de zonas pantanosas y barro.
Las Aeromonas no son consideradas organismos marinos, pero pueden ser encontrados naturalmente en sistemas marinos en su interfase con el agua dulce (estuarios, desembocaduras de ríos en el mar). Sobreviven incluso a altas concentraciones de sal. Usualmente no son parte de la población bacteriana autóctona del agua subterránea, que normalmente es pobre en nutrientes. Sin embargo, Aeromonas sp pueden desarrollar en agua rica en un gran número de nutrientes, alcanzando un pico los meses de verano, tanto en lagos de agua dulce como aguas cloradas para beber. Mientras no sea considerada de origen fecal, estos organismos son tolerados como polutantes. La presencia de Aeromonas sp en alimentos refleja más probablemente el contacto de esos alimentos con agua, como es reflejado por el nombre de especies de tipo A. hydrofila, que significa “que ama el agua”.
Las infecciones humanas eran consideradas oportunistas, solo capaces de infectar individuos inmunocomprometidos. Sin embargo ahora se acepta que pueden causar un amplio rango de enfermedades extraintestinales en inmunocompetentes.
Hay controversia en cuanto al rol de Aeromonas en diarrea y enfermedad gastrointestinal; el aislamiento de Aeromonas en muchos pacientes asintomáticos ha sido problemático en cuanto a asignarle un rol, pero también se la ha aislado en pacientes con diarrea, de manera análoga a la Escherichia coli, por lo tanto la interpretación debe contextualizarse en la clínica y el laboratorio de un paciente determinado.
Manifestaciones Clínicas:
Aunque la enfermedad diarreica es probablemente la manifestación más común de infección por Aeromons, el organismo ha estado asociado a una variedad de presentaciones clínicas que van desde la infección de heridas hasta la bacteriemia.
Diarrea:
Aeromona sp está asociada a una variedad de presentaciones diarreicas que incluyen:
• Diarrea secretoria aguda, a menudo acompañada de vómitos.
• Diarrea disentérica aguda con sangre y moco.
• Diarrea crónica que dura más de 10 días.
• Diarrea colérica con heces en agua de arroz.
• Diarrea del viajero.
Ha habido descripciones de A. hydrophila asociada a síndrome urémico hemolítico.
Infección de heridas:
• Diarrea secretoria aguda, a menudo acompañada de vómitos.
• Diarrea disentérica aguda con sangre y moco.
• Diarrea crónica que dura más de 10 días.
• Diarrea colérica con heces en agua de arroz.
• Diarrea del viajero.
Ha habido descripciones de A. hydrophila asociada a síndrome urémico hemolítico.
Infección de heridas:
Aeromonas es capaz de causar leves a severas infecciones de heridas. Las infecciones invariablemente afectan a exposiciones traumáticas recientes, generalmente en extremidades. Virtualmente todas las infecciones de heridas son adquiridas en la comunidad y afectan a los hombres tres veces más frecuentemente que a las mujeres. La presentación más típica es la celulitis, aunque se han descripto también mionecrosis con o sin producción de gas, rabdomiolisis, y lesiones que mimetizan el ectima gangrenoso.
A. hydrophila, A. veronii, y A. schubertii son las especies más comúnmente aisladas de infecciones de heridas. Aeromonas fue un patógeno común aislado de heridas entre las víctimas del tsunami en diciembre de 2004, y un número elevado de Aeromonas sp fueronreportadas en New Orleans después del huracán Katrina.
Las infecciones serias de heridas y la sepsis se han reportado después del uso medicinal de sanguijuelas. Las aeromonas residen en el intestino de la sanguijuela Hirudo medicinales, donde ayudan a la digestión enzimática de la sangre ingerida por la sanguijuela.
Bacteriemia:
La sepsis por especies de Aeromonas están fuertemente asociadas con una infección por Aeromonas veronii biovar sobria (antiguamente identificada simplemente como Aeromonas sobria en la literatura clínica). Estos pacientes se presentan con los signos y síntomas clásicos de la sepsis por gram negativos.
Casi todos los pacientes tienen fiebre, y frecuentemente exhiben síntomas gastrointestinales incluyendo dolor abdominal, náuseas, vómitos y diarrea; también han sido descriptas las infecciones extraintestinales. La enfermedad tiende a ocurrir en hombres mayores con neoplasias hematológicas, enfermedades hepáticas serias, o injurias traumáticas. Sin embargo hay casos descriptos de sepsis debida a A. hydrophila productoras de bete lactamasas de espectro extendido en pacientes pediátricos con diarrea y neumonía.
No siempre es posible identificar el origen del organismo en casos de sepsis; en tales casos, es razonable suponer que fue adquirida del tracto gastrointestinal, análoga a la “sepsis primaria” causada por especies de vibrio no coléricos (por ej V. vulnificus).
Sitios extraintestinales misceláneos: Aeromonas sp ha estado implicada en casos de infecciones oculares, osteomielitis, meningitis, infecciones respiratorias después de “casi ahogamientos”, abscesos pélvicos, otitis, cistitis, endocarditis, peritonitis, colecistitis, e infecciones articulares. Se han reportado también fascitis necrotizantes causados por A. hydrophila.
Diagnóstico:
Aeromonas sp puede ser generalmente identificada en laboratorios de microbiología como bacilo gram negativo anaerobio facultativo, fermentador de glucosa, polar, flagelado, oxidasa positivo, y resistente al agente vibriostático O/129 e incapaz de crecer en cloruro de sodio al 6,5%. Aeromona crece en la mayoría de los medios de cultivo usados de rutina como en los medios para coprocultivo. La hemólisis en agar sangre es variable, con la mayoría de las especies mostrando beta hemólisis.
Aeromonas no son buscadas rutinariamente en la mayoría de los laboratorios como parte del protocolo para aislamiento de patógenos fecales. En casos de enfermedad diarreica en que puede ser un organismo infectante, el laboratorio debe ser aconsejado para buscar Aeromonas.
La identificación definitiva se cumple con un pequeño número de tests bioquímicos y marcadores antimicrobianos usando el llamado Aerokey II. Cuando se usan en conjunto con los tests adicionales, el microbiólogo debe ser capaz de identificar todas las especies de Aeromonas. Sin embargo la diferenciación en especies es a menudo errónea por carencia de marcadores discriminatorios específicos entre ellas.
Tratamiento:
La mayoría de los casos de diarrea asociada a aAeromonas son autolimitadas y pueden ser manejadas con terapia de sostén, incluyendo hidratación oral o intravenosa. Los antibióticos pueden ser útiles en pacientes pediátricos o en gerontes e inmunocomprometidos (o en casos severos en adultos sanos). Deben usarse antibióticos en infecciones de heridas y en sepsis.
La mayoría de las cepas son resistentes a penicilina, ampicilina, carbenicilina, ticarcilina, y sensibles a cefalosporinas de 2º y 3º generación, aminoglucósidos, carbapenems, cloramfenicol, tetraciclinas, trimetoprima-sulfametoxazol, y fluoroquinolonas.
Recomendaciones: Basados en observaciones, la terapia empírica inicial de infecciones sospechosas de Aeromonas debe incluir fluoroquinolona, o TMS hasta tener los tests de sensibilidad.
Prevención: Basados en la relación del microorganismo con su hábitat natural acuático, el riesgo de infección puede ser reducido por evitar la ingestión de agua de fuente natural y evitar la contaminación con agua de heridas traumáticas, particularmente en los meses de verano.
Infección por Vibrio vulnificus.
El Vibrio vulnificus es una bacteria gram negativa de la familia Vibrio, que puede causar septicemia, seria infección de heridas, y diarrea. Es la causa más importante de muerte asociada a mariscos en los EE UU. La infección debida a V vulnificus es la más común en individuos que tienen enfermedades crónicas de base, con un riesgo mayor entre aquellas que padecen enfermedades hepáticas o hemocromatosis.
A. hydrophila, A. veronii, y A. schubertii son las especies más comúnmente aisladas de infecciones de heridas. Aeromonas fue un patógeno común aislado de heridas entre las víctimas del tsunami en diciembre de 2004, y un número elevado de Aeromonas sp fueronreportadas en New Orleans después del huracán Katrina.
Las infecciones serias de heridas y la sepsis se han reportado después del uso medicinal de sanguijuelas. Las aeromonas residen en el intestino de la sanguijuela Hirudo medicinales, donde ayudan a la digestión enzimática de la sangre ingerida por la sanguijuela.
Bacteriemia:
La sepsis por especies de Aeromonas están fuertemente asociadas con una infección por Aeromonas veronii biovar sobria (antiguamente identificada simplemente como Aeromonas sobria en la literatura clínica). Estos pacientes se presentan con los signos y síntomas clásicos de la sepsis por gram negativos.
Casi todos los pacientes tienen fiebre, y frecuentemente exhiben síntomas gastrointestinales incluyendo dolor abdominal, náuseas, vómitos y diarrea; también han sido descriptas las infecciones extraintestinales. La enfermedad tiende a ocurrir en hombres mayores con neoplasias hematológicas, enfermedades hepáticas serias, o injurias traumáticas. Sin embargo hay casos descriptos de sepsis debida a A. hydrophila productoras de bete lactamasas de espectro extendido en pacientes pediátricos con diarrea y neumonía.
No siempre es posible identificar el origen del organismo en casos de sepsis; en tales casos, es razonable suponer que fue adquirida del tracto gastrointestinal, análoga a la “sepsis primaria” causada por especies de vibrio no coléricos (por ej V. vulnificus).
Sitios extraintestinales misceláneos: Aeromonas sp ha estado implicada en casos de infecciones oculares, osteomielitis, meningitis, infecciones respiratorias después de “casi ahogamientos”, abscesos pélvicos, otitis, cistitis, endocarditis, peritonitis, colecistitis, e infecciones articulares. Se han reportado también fascitis necrotizantes causados por A. hydrophila.
Diagnóstico:
Aeromonas sp puede ser generalmente identificada en laboratorios de microbiología como bacilo gram negativo anaerobio facultativo, fermentador de glucosa, polar, flagelado, oxidasa positivo, y resistente al agente vibriostático O/129 e incapaz de crecer en cloruro de sodio al 6,5%. Aeromona crece en la mayoría de los medios de cultivo usados de rutina como en los medios para coprocultivo. La hemólisis en agar sangre es variable, con la mayoría de las especies mostrando beta hemólisis.
Aeromonas no son buscadas rutinariamente en la mayoría de los laboratorios como parte del protocolo para aislamiento de patógenos fecales. En casos de enfermedad diarreica en que puede ser un organismo infectante, el laboratorio debe ser aconsejado para buscar Aeromonas.
La identificación definitiva se cumple con un pequeño número de tests bioquímicos y marcadores antimicrobianos usando el llamado Aerokey II. Cuando se usan en conjunto con los tests adicionales, el microbiólogo debe ser capaz de identificar todas las especies de Aeromonas. Sin embargo la diferenciación en especies es a menudo errónea por carencia de marcadores discriminatorios específicos entre ellas.
Tratamiento:
La mayoría de los casos de diarrea asociada a aAeromonas son autolimitadas y pueden ser manejadas con terapia de sostén, incluyendo hidratación oral o intravenosa. Los antibióticos pueden ser útiles en pacientes pediátricos o en gerontes e inmunocomprometidos (o en casos severos en adultos sanos). Deben usarse antibióticos en infecciones de heridas y en sepsis.
La mayoría de las cepas son resistentes a penicilina, ampicilina, carbenicilina, ticarcilina, y sensibles a cefalosporinas de 2º y 3º generación, aminoglucósidos, carbapenems, cloramfenicol, tetraciclinas, trimetoprima-sulfametoxazol, y fluoroquinolonas.
Recomendaciones: Basados en observaciones, la terapia empírica inicial de infecciones sospechosas de Aeromonas debe incluir fluoroquinolona, o TMS hasta tener los tests de sensibilidad.
Prevención: Basados en la relación del microorganismo con su hábitat natural acuático, el riesgo de infección puede ser reducido por evitar la ingestión de agua de fuente natural y evitar la contaminación con agua de heridas traumáticas, particularmente en los meses de verano.
Infección por Vibrio vulnificus.
El Vibrio vulnificus es una bacteria gram negativa de la familia Vibrio, que puede causar septicemia, seria infección de heridas, y diarrea. Es la causa más importante de muerte asociada a mariscos en los EE UU. La infección debida a V vulnificus es la más común en individuos que tienen enfermedades crónicas de base, con un riesgo mayor entre aquellas que padecen enfermedades hepáticas o hemocromatosis.
Epidemiología:
V vulnificus existe como bacteria que vive libremente, habitando microambientes marinos o aguas estuarinas. Actualmente se reconocen tres biotipos: el biotipo 1, que da cuenta de casi todas las infecciones humanas; el biotipo 2 que es patógeno de la anguila; y el biotipo 3 , un aparente biotipo híbrido entre 1 y 2 que ha sido descripto en mojarras y asociado a infección de heridas en Israel.
Las ostras concentran la mayor cantidad de V vulnificus por su modo de alimentación provista de filtro, y hay regiones del mundo en las que tienen 100% de infestación. Más del 90% de los pacientes con septicemia “primaria” por V vulnificus (septicemia sin una puerta de entrada obvia) tienen el antecedente de haber consumido ostras antes del inicio de la enfermedad.
La infección de heridas dan cuenta del 25% de las infecciones por V. vulnificus. Esas infecciones generalmente resultan de la exposición de heridas a aguas saladas o salitrosas que contienen el microorganismo, y más a menudo ocurren en el contexto de la manipulación de frutos del mar o en asociación con actividades acuáticas recreacionales. Como con las ostras, u otras infecciones asociadas a otras enfermedades por ingesta de frutos del mar, las infecciones de heridas son más frecuentes durante el verano. En agosto de 2005 después del huracán Katrina aumentó la frecuencia de infecciones d eheridas por V. vulnificus. La mayoría de los casos ocurrieron entre individuos con condiciones médicas predisponentes y exposición de heridas a aguas de inundación.
Los grupos de riesgo de infecciones serias por V. vulnificus incluye:
• Cirrosis alcohólica.
• Enfermedades hepáticas incluyendo cirrosis y hepatitis crónica.
• Consumo de alcohol sin enfermedad hepática documentada.
• Hemocromatosis hereditaria.
• Enfermedades crónicas tales como diabetes mellitus, artritis reumatoidea, talasemia mayor, insuficiencia renal crónica, y linfoma.
La incidencia de las infecciones combinadas por V. vulnificus es de 0,5/100.000/año.
Patogénesis:
La virulencia de V. vulnificus ha estado asociada con tres factores mayores: 1) producción de una cápsula polisacárida anti-fagocítica; 2) la toxina RtxA; y 3) disponibilidad de hierro y sistemas de incorporación de hierro.
Cápsula/LPS. V. vulnificus produce un polisacárido capsular que le brinda protección contra la fagocitosis y la opsonización. Las cepas de V. vulnificus son capaces de someterse a fases de variación, variando entre las formas capsuladas (colonias opacas) y las formas no encapsuladas (colonias translúcidas). Las cepas no encapsuladas son avirulentas en modelos de ratones. Cuando esas cepas son incorporadas por las ostras se produce un viraje a la forma capsulada o virulenta del microorganismo.
Los anticuerpos anticapsulares son protectores pero parecen ser tipo específicos más que de reacción cruzada. La naturaleza protectiva tipo específica de los anticuerpos es de significación, ya que V vulnificus tiene una gran diversidad en tipos capsulares. Hay 96 diferentes tipos capsulares (“carbotipos”).
V. vulnificus contiene un lipopolisacárido (LPS) pero, en contraste con Escherichia coli y otros miembros de las Enterobacteriaceae, el LPS de V. vulnificus no es un fuerte disparador de la liberación de TNF (factor de necrosis tumoral)-alfa y otras citoquinas relacionadas a shock. Sin embargo, el polisacárido capsular en si mismo puede directamente disparar alguna respuesta de citoquinas, contribuyendo al desarrollo del síndrome de shock. El TNF-alfa fue detectado en ratones hasta 12 horas después de la inoculación de V. vulnificus encapsulado, mientras que las cepas no encapsuladas fueron rápidamente aclaradas. Tanto el polisacárido capsular como LPS provocó liberación de citoquinas in vitro por parte de las células mononucleares periféricas.
Toxinas.
V. vulnificus produce una variedad de toxinas extracelulares, incluyendo tanto hemolisinas como proteasas, aunque la eliminación de esas toxinas de la bacteria no afecta la virulencia en modelos de ratón.
La virulencia ha estado asociada a RtxA1, una toxina homóloga a las toxinas formadoras de poros RTX encontrada en Vibrio cólera y otras bacterias gram negativas. Esta toxina parece actuar vía Nox 1 para inducir generación de especies reactivas del oxígeno en las células epiteliales del intestino, produciendo muerte celular.
Hierro.
La virulencia ha estado asociada a RtxA1, una toxina homóloga a las toxinas formadoras de poros RTX encontrada en Vibrio cólera y otras bacterias gram negativas. Esta toxina parece actuar vía Nox 1 para inducir generación de especies reactivas del oxígeno en las células epiteliales del intestino, produciendo muerte celular.
Hierro.
El crecimiento de V. vulnificus es dependiente en parte de la disponibilidad de hierro. El crecimiento del microorganismo en el suero humano está relacionado al porcentaje de saturación de la transferrina. Cuando la saturación de la transferrina excede 70%, el crecimiento de la bacteria es casi exponencial.
La relación entre el hierro y la virulencia en V vulnificus puede explicar la susceptibilidad a infecciones serias con este microorganismo en pacientes con hemocromatosis. Sin embargo, la mayoría de los pacientes con infecciones serias por V vulnificus tienen niveles de hierro y saturación normales.
Manifestaciones Clínicas.
V vulnificus causa infección de heridas y “septicemia primaria” (septicemia sin un foco claro de origen de la infección, tal como heridas). La infección de heridas puede ser adquirida durante el manejo de mariscos o pescados, o después de exposición de una herida preexistente a aguas estuarinas.
V. vulnificus ha estado asociado a gastroenteritis. Sin embargo, un rol etiológico es dificultoso de establecer cuando el microorganismo es aislado de la materia fecal, ya que la bacteria es ubicua tanto en agua dulce como en mariscos.
Infección de heridas:
La relación entre el hierro y la virulencia en V vulnificus puede explicar la susceptibilidad a infecciones serias con este microorganismo en pacientes con hemocromatosis. Sin embargo, la mayoría de los pacientes con infecciones serias por V vulnificus tienen niveles de hierro y saturación normales.
Manifestaciones Clínicas.
V vulnificus causa infección de heridas y “septicemia primaria” (septicemia sin un foco claro de origen de la infección, tal como heridas). La infección de heridas puede ser adquirida durante el manejo de mariscos o pescados, o después de exposición de una herida preexistente a aguas estuarinas.
V. vulnificus ha estado asociado a gastroenteritis. Sin embargo, un rol etiológico es dificultoso de establecer cuando el microorganismo es aislado de la materia fecal, ya que la bacteria es ubicua tanto en agua dulce como en mariscos.
Infección de heridas:
V. vulnificus puede contaminar heridas expuestas a aguas estuarinas, mariscos o pescados. Los ejemplos típicos incluyen heridas en las manos relacionadas a la apertura de ostras, o laceraciones relacionadas a entrada o salida de lanchas al mar o a botamiento de embarcaciones. Las infecciones son usualmente leves. Sin embargo, en pacientes de alto riesgo, la infección puede diseminarse rápidamente, produciendo severa miositis y fascitis que recuerda la gangrena gaseosa. (Figura 1)

Figura 1. Lesión extensiva bullosa hemorrágica en un paciente con septicemia por Vibrio vulnificus. La mortalidad excede en estos casos el 50%.
Septicemia primaria.
La septicemia primaria por Vibrio vulnificus está asociada con ingestión de mariscos mal cocidos, particularmente ostras crudas. Los pacientes con septicemia primaria generalmente presentan enfermedades hepáticas de base, alcoholismo, hemocromatosis hereditaria o enfermedades crónicas como se dijo antes.
Aproximadamente un tercio de los pacientes con septicemia primaria se presentan con shock o se ponen hipotensos después de las 12 horas d einternación. Tres cuartas partes de los pacientes tienen lesiones bullosas en piel (Figura 2). La trombocitopenia es común, y a menudo hay evidencias de coagulación intravascular diseminada. Complicaciones tales como hemorragia digestiva no son raras.
Figura 2. Lesiones bullosas típicas son vistas en el 75% de los pacientes con infección con V. vulnificus.
La septicemia primaria por V vulnificus es una enfermedad seria con alta mortalidad como se ilustra en las siguientes observaciones:
• De todas las infecciones adquiridas por ingesta de alimentos, la infección por V vulnificus es la de mayor tasa de mortalidad (39%).
• Mortalidad excediendo 40% han sido reportadas, con más de 90% de mortalidad en aquellos que evolucionaron a hipotensión.
Las personas que sobreviven al shock, a menudo requieren hospitalización prolongada en unidades de cuidados intensivos, con complicaciones resultantes de fallo multiorgánico.
Diagnóstico:
Dada la potencial severidad de la infección, un diagnóstico presuntivo de septicemia por V. vulnificus debe ser hecho en cualquier persona con shock séptico, características lesiones bullosas en piel, y factores de riesgo para adquirir esta infección. La infección debe ser sospechada en una persona que está en un grupo de riesgo que tiene una infección de herida rápidamente progresiva asociada a exposición a aguas estuarinas.
El diagnóstico se confirma por cultivo. V. vulnificus crecerá sin dificultad en medios de cultivo standard o en medios no selectivos (tales como agar sangre) rutinariamente usados para cultivos de heridas; la identificación y caracterización en especie del microorganismo es posible a través de cualquier sistema de identificación microbiológico disponibles comercialmente.
Como con todas las especies de Vibrio, el aislamiento del organismo de la materia fecal, requiere el uso de medios de cultivo selectivos (tiosulfato citrato sales biliares sucrosa(TCBS)), en los que V. vulnificus, V parahaemolyticus y alguna otra especie de Vibrio (pero no V cólera) producen típicas colonias verde-azuladas.
Terapia.
Los casos fatales de septicemia o de infección seria de heridas por V. vulnificus han mostrado aumentar en relación al retraso diagnóstico, y entre el comienzo de la enfermedad y la iniciación de la terapia antibiótica. Por eso, los pacientes con sospecha, o diagnóstico presuntivo de septicemia por V. vulnificus (definidos más arriba), deben comenzar inmediatamente con antibióticos, y deben ser manejados agresivamente en una unidad de cuidados intensivos, para minimizar las posibles consecuencias de la hipotensión, del shock séptico, y el riesgo de fallo multiorgánico.
Estudios in vitro han mostrado un aparente sinergismo entre minociclina y cefotaxima en el tratamiento de infecciones serias por V. vulnificus. Recientemente se han probado las nuevas quinolonas. De esas observaciones surge que los regímenes que incluyan una tetraciclina son más efectivas. Por lo tanto, los pacientes con septicemia o infección seria de heridas deben ser tratados con una combinación que incluya una tetraciclina por vía oral como minociclina o doxiciclina 100 mg dos veces por día más cefotaxime 2 gr IVcada 8 hs, o ceftriaxona 1 gr IV por día ajustados y a la función hepática y renal. Una alternativa razonable es levofloxacina 500 mg una vez por día.
Las infecciones leves en pacientes que no pertenecen a grupos de riesgo pueden responder a terapia local y antibióticos por vía oral. En pacientes de alto riesgo, lsa infecciones serias d eheridas pueden requerir debridamiento agresivo además de antibióticos parenterales.
Prevención.
Dada la alta mortalidad asociada a infecciones por V. vulnificus, las personas en alto riesgo deben evitar comer mariscos mal cocidos, particularmente ostras, y deben evitar situaciones donde puedan ocurrir heridas en contacto con aguas estuarinas. Como ejemplo, es desaconsejable que un paciente en tratamiento con quimioterapia en el nadir de su recuento celular vaya a pescar en aguas estuarinas.
Hay terapias nuevas tal como el uso de bacteriófagos y la inmunoterapia con antisuero contra polisacárido de V. vulnificus conjugada con vacuna de toxoide tetánico, que han mostrado efectividad en modelos animales.
Infecciones por Erysipelothrix.
Introducción: Erysipelothrix rhusiopathiae, un bacilo pleomórfico gram positivo, causa tanto una enfermedad autolimitada de partes blandas como una seria infección sistémica. E. rhusiopathiae está distribuido ampliamente en la naturaleza, e infecta animales, tales como cerdos que puede ser el mayor reservorio del microorganismo. Erysipelothrix es encontrado también en ovejas, caballos, vacas, pollos, cangrejos, peces, perros y gatos.
Las infecciones en humanos son usualmente debidas a exposición ocupacional. Así, los trabajadores de mataderos, carniceros, pescadores, granjeros, y veterinarios están en riesgo de infectarse con E. rhusiopathiae.

Figura 1. Lesión extensiva bullosa hemorrágica en un paciente con septicemia por Vibrio vulnificus. La mortalidad excede en estos casos el 50%.
Septicemia primaria.
La septicemia primaria por Vibrio vulnificus está asociada con ingestión de mariscos mal cocidos, particularmente ostras crudas. Los pacientes con septicemia primaria generalmente presentan enfermedades hepáticas de base, alcoholismo, hemocromatosis hereditaria o enfermedades crónicas como se dijo antes.
Aproximadamente un tercio de los pacientes con septicemia primaria se presentan con shock o se ponen hipotensos después de las 12 horas d einternación. Tres cuartas partes de los pacientes tienen lesiones bullosas en piel (Figura 2). La trombocitopenia es común, y a menudo hay evidencias de coagulación intravascular diseminada. Complicaciones tales como hemorragia digestiva no son raras.

Figura 2. Lesiones bullosas típicas son vistas en el 75% de los pacientes con infección con V. vulnificus.
La septicemia primaria por V vulnificus es una enfermedad seria con alta mortalidad como se ilustra en las siguientes observaciones:
• De todas las infecciones adquiridas por ingesta de alimentos, la infección por V vulnificus es la de mayor tasa de mortalidad (39%).
• Mortalidad excediendo 40% han sido reportadas, con más de 90% de mortalidad en aquellos que evolucionaron a hipotensión.
Las personas que sobreviven al shock, a menudo requieren hospitalización prolongada en unidades de cuidados intensivos, con complicaciones resultantes de fallo multiorgánico.
Diagnóstico:
Dada la potencial severidad de la infección, un diagnóstico presuntivo de septicemia por V. vulnificus debe ser hecho en cualquier persona con shock séptico, características lesiones bullosas en piel, y factores de riesgo para adquirir esta infección. La infección debe ser sospechada en una persona que está en un grupo de riesgo que tiene una infección de herida rápidamente progresiva asociada a exposición a aguas estuarinas.
El diagnóstico se confirma por cultivo. V. vulnificus crecerá sin dificultad en medios de cultivo standard o en medios no selectivos (tales como agar sangre) rutinariamente usados para cultivos de heridas; la identificación y caracterización en especie del microorganismo es posible a través de cualquier sistema de identificación microbiológico disponibles comercialmente.
Como con todas las especies de Vibrio, el aislamiento del organismo de la materia fecal, requiere el uso de medios de cultivo selectivos (tiosulfato citrato sales biliares sucrosa(TCBS)), en los que V. vulnificus, V parahaemolyticus y alguna otra especie de Vibrio (pero no V cólera) producen típicas colonias verde-azuladas.
Terapia.
Los casos fatales de septicemia o de infección seria de heridas por V. vulnificus han mostrado aumentar en relación al retraso diagnóstico, y entre el comienzo de la enfermedad y la iniciación de la terapia antibiótica. Por eso, los pacientes con sospecha, o diagnóstico presuntivo de septicemia por V. vulnificus (definidos más arriba), deben comenzar inmediatamente con antibióticos, y deben ser manejados agresivamente en una unidad de cuidados intensivos, para minimizar las posibles consecuencias de la hipotensión, del shock séptico, y el riesgo de fallo multiorgánico.
Estudios in vitro han mostrado un aparente sinergismo entre minociclina y cefotaxima en el tratamiento de infecciones serias por V. vulnificus. Recientemente se han probado las nuevas quinolonas. De esas observaciones surge que los regímenes que incluyan una tetraciclina son más efectivas. Por lo tanto, los pacientes con septicemia o infección seria de heridas deben ser tratados con una combinación que incluya una tetraciclina por vía oral como minociclina o doxiciclina 100 mg dos veces por día más cefotaxime 2 gr IVcada 8 hs, o ceftriaxona 1 gr IV por día ajustados y a la función hepática y renal. Una alternativa razonable es levofloxacina 500 mg una vez por día.
Las infecciones leves en pacientes que no pertenecen a grupos de riesgo pueden responder a terapia local y antibióticos por vía oral. En pacientes de alto riesgo, lsa infecciones serias d eheridas pueden requerir debridamiento agresivo además de antibióticos parenterales.
Prevención.
Dada la alta mortalidad asociada a infecciones por V. vulnificus, las personas en alto riesgo deben evitar comer mariscos mal cocidos, particularmente ostras, y deben evitar situaciones donde puedan ocurrir heridas en contacto con aguas estuarinas. Como ejemplo, es desaconsejable que un paciente en tratamiento con quimioterapia en el nadir de su recuento celular vaya a pescar en aguas estuarinas.
Hay terapias nuevas tal como el uso de bacteriófagos y la inmunoterapia con antisuero contra polisacárido de V. vulnificus conjugada con vacuna de toxoide tetánico, que han mostrado efectividad en modelos animales.
Infecciones por Erysipelothrix.
Introducción: Erysipelothrix rhusiopathiae, un bacilo pleomórfico gram positivo, causa tanto una enfermedad autolimitada de partes blandas como una seria infección sistémica. E. rhusiopathiae está distribuido ampliamente en la naturaleza, e infecta animales, tales como cerdos que puede ser el mayor reservorio del microorganismo. Erysipelothrix es encontrado también en ovejas, caballos, vacas, pollos, cangrejos, peces, perros y gatos.
Las infecciones en humanos son usualmente debidas a exposición ocupacional. Así, los trabajadores de mataderos, carniceros, pescadores, granjeros, y veterinarios están en riesgo de infectarse con E. rhusiopathiae.
Patogénesis:
Poco se sabe sobre la patogenia de la infección por E. rhusiopathiae. Las siguientes observaciones se han hecho en estudios en animales in vitro:
• Los organismos virulentos tienen una cápsula que es antifagocítica y puede contribuir a la sobrevida intracelular (en ausencia de opsonización con un anticuerpo específico).
• La sobrevida intracelular de un organismo virulento en macrófagos está asociado a reducción de la estimulación de la explosión respiratoria oxidativa.
• La proteína SpaA es un antígeno de superficie de E. rhusiopathiae. El significado patogénico de esta proteína fue sugerida en un modelo de ratón en que el anticuerpo contra SpaA fue protector contra cambios letales.
• La enzima neuraminidasa puede contribuir a la patogenicidad de Erysipelothrix, ya que es capaz de producir inflamación y edema en modelos animales en conejos.
Manifestaciones Clínicas.
El espectro clínico de las infecciones humanas incluye:
• Infección cutánea localizada.
• Enfermedad cutánea difusa.
• Infección hematógena sistémica.

Infección por Erysipelothryx rhusiopathiae
Erisipeloide. Infección causada pE.
Infección Cutánea Localizada.
La forma localizada cutánea de enfermedad, conocida como erysipeloide de Rosenbach, es la más común de las infecciones humanas debidas a E. rhusiopathiae. Los dedos y/o las manos (el sitio de exposición) están usualmente afectados en esta infección. Como ejemplo, el erisipeloide ha sido descripto en los dedos o manos de pescadores, o empaquetadores de mariscos que sufren traumas menores mientras manipulan langostinos, cangrejos o pescados.
La infección puede ser consecuencia de mordeduras de perros o gatos.
Inicialmente, puede haber dolor leve en el sitio de la inoculación, seguido por un dolor pulsante, prurito, sensación de quemadura, y pinchazos. La lesión típica de piel, progresa lentamente desde un punto rojo en el sitio de inoculación, hasta la característica lesión de erisipelide de piel, que consiste en un centro purpúrico con un borde elevado.
La forma localizada cutánea de enfermedad, conocida como erysipeloide de Rosenbach, es la más común de las infecciones humanas debidas a E. rhusiopathiae. Los dedos y/o las manos (el sitio de exposición) están usualmente afectados en esta infección. Como ejemplo, el erisipeloide ha sido descripto en los dedos o manos de pescadores, o empaquetadores de mariscos que sufren traumas menores mientras manipulan langostinos, cangrejos o pescados.
La infección puede ser consecuencia de mordeduras de perros o gatos.
Inicialmente, puede haber dolor leve en el sitio de la inoculación, seguido por un dolor pulsante, prurito, sensación de quemadura, y pinchazos. La lesión típica de piel, progresa lentamente desde un punto rojo en el sitio de inoculación, hasta la característica lesión de erisipelide de piel, que consiste en un centro purpúrico con un borde elevado.

Erisipeloide de Rosenbach.
Los pacientes infectados se quejan típicamente de rigidez y dolor en los dedos afectados a pesar de una mínima inflamación. La linfangitis local y la adenitis se ve en 30% de los casos. La mayoría de las infecciones localizadas se resuelven aún en ausencia de tarapia específica. Síntomas sistémicos tales como fiebre alta o escalofríos son infrecuentes, y ocurren en el 6% de los casos.
Un diagnóstico provisional puede ser hecho por el antecedente de contacto con materiales potencialmente contaminados o exposición ocupacional, asociado a los hallazgos típicos.
La tinción de Gram y el cultivo del material aspirado son a menudo negativos debido a que el organismo está ubicado profundamente en la dermis.
Un diagnóstico provisional puede ser hecho por el antecedente de contacto con materiales potencialmente contaminados o exposición ocupacional, asociado a los hallazgos típicos.
La tinción de Gram y el cultivo del material aspirado son a menudo negativos debido a que el organismo está ubicado profundamente en la dermis.
Enfermedad Cutánea Difusa.
El erisipeloide ocasionalmente progresa a enfermedad cutánea difusa en pacientes no tratados. Comer carne contaminada ha estado asociada a este cuadro.
La enfermedad cutánea difusa se caracteriza por lesiones purpúricas cutáneas que se expanden con un centro claro. Lesiones bullosas en el sitio primario o en un sitio distante del primario pueden ser vistas. Esos pacientes a menudo tienen manifestaciones sistémicas como fiebre alta y artralgias. Los hemocultivos son negativos.
Infección Sistémica.
La infección bacteriémica, con o sin endocarditis, es usualmente una infección primaria más que una diseminación desde una lesión cutánea localizada; sin embargo, aproximadamente 40% de los pacientes con infección sistémica tienen lesiones en piel sugestivas de erisipeloide. La bacteriemia persistente ha sido observada después de la ingestión de mariscos contaminados o cerdo mal cocido.
La mayoría de los pacientes se presentan con fiebre de 2 o 3 semanas de duración. Lesiones cutáneas serpiginosas o múltiples lesiones bullosas en el tronco y extremidades se ven frecuentemente. La fiebre y los escalofríos pueden resolverse espontáneamente pero pueden recurrir.
Una presentación clínica que recuerda la sepsis por gram negativos puede ser vista en pacientes con enfermedad hepática o cardíaca severas de base. Más de un tercio de los pacientes con infecciones sistémicas son alcohólicos, y hepatópatas crónicos como factores predisponentes importantes. La bacteriemia es vista en inmunocomprometidos, especialmente aquellos que reciben corticosteroides y/o terapia citotóxica por colagenopatías o neoplasias.
Endocarditis.
La bacteriemia por E. rhusiopathiae está usualmente asociada a severa enfermedad clínica y a menudo se complica con endocarditis. Casi todos los reportes han sido en válvulas nativas no protésicas, con propensión al compromiso de la válvula aórtica.
El diagnóstico de endocarditis se establece en base a la historia clínica, el examen físico, laboratorio e imágenes. Los criterios de Duke son usados típicamente para establecer el diagnóstico. La ausencia inicial de hallazgos clínicos o ecocardiográficos de endocarditis no excluye el diagnóstico en pacientes con hemocultivos positivos. Tales pacientes pueden tener un número de criterios menores de Duke para realizar el diagnóstico de endocarditis.
La endocarditis por Erysipelothrix frecuentemente produce destrucción extensa de las válvulas cardíacas, y hasta un tercio de los pacientes requieren reemplazo valvular. Las complicaciones de la endocarditis por Erysipelothrix incluyen fallo renal agudo por glomerulonefritis proliferativa.
Otros.
Otras complicaciones debidas a infección por E. rhusiopathiae incluyen artritis séptica (probablemente relacionada a bacteriemia), fascitis necrotizante debido a inoculación local, y peritonitis en pacientes que reciben diálisis peritoneal y tienen bacteriemia.
Diagnóstico.
Los medios de cultivo comercialmente disponibles son satisfactorios para el aislamiento en sangre de E. rhusiopathiae, ya que este no es un organismo fastidioso, y el crecimiento es reconocido en 2 o 3 días. Sin embargo, puede haber errores en la identificación, y a veces este microorganismo puede ser confundido con Lactobacillus o aún especies de Enterococos.
Tratamiento.
Las lesiones de erisipeloide pueden resolverse espontáneamente dentro de tres semanas. Sin embargo, una terapia antibiótica apropiada acorta la enfermedad clínica y previene la recidiva. Además, la terapia local con calor y reposo puede ser útil para el paciente con artritis y lesiones inflamadas y dolorosas, La incisión quirúrgica o el debridamiento de las lesiones no está indicado.
Penicilina e imipenem son los antibióticos más activos contra E. rhusiopathiae in vitro. Además, la penicilina ha mostrado ser efectiva para todas las formas clínicas de infección por Erysipelothrix.
Otras drogas son también activas, como fluoroquinolonas, clindamicina y daptomicina.
Macrólidos, tetraciclinas, y cloramfenicol, no son activas consistentemente y no deben usarse en infecciones diseminadas.
E. rhusiopathiae es resistente a sulfas, TMS, vancomicina.
En resumen, para las formas cutáneas localizadas se recomienda penicilina V 500 mg/6 hs, o si el paciente es alérgico ciprofloxacina 250 mg/12 hs, o eritromicina 500 mg/6hs
durante 7 días.
Para las formas cutáneas severas o para infecciones sistémicas se recomienda penicilina G 2 a 4 millones cada 4 hs o ceftriaxona 2 gr 1 vez por día, o imipenem 500 mg cada 6 hs, o una fluoroquinolona como ciprofloxacina 400 mg cada 12 hs o levofloxacina 500 mg una vez por día.
Los pacientes con bacteriemia o endocarditis deben ser tratados al menos 4 semanas con ATB parenterales.
Infecciones por Mycobacterium Marinum.
Mycobacterium marinum es una especie de micobacteria atípica, encontrada en aguas calientes o frias, dulces o saladas. La infección por M. marinum ocurre siguiendo a traumas de piel y partes blandas que son expuestas a un medio ambiente acuático o a animales marinos. La infección se presenta usualmente como un granuloma localizado pero puede producir linfangitis ascendente que recuerda la esporotricosis, o puede diseminarse a tejidos más profundos. M. marinum es un patógeno clasificado como grupo 1 de Runyon y es un fotocromógeno, lo que significa que produce pigmento cuando es cultivado y expuesto a la luz. El crecimiento en cultivo ocurre en 7 a 14 días, óptimamente a 32ºC.
Patogenia.
M. marinum es una especie de micobacteria atípica de medio acuático que comúnmente infecta peces y anfibios. Fue reconocido por primera vez como causal de infección humana en 1951. La infección con M. marinum generalmente como complicación de una herida de piel o partes blandas expuestas a equipos acuáticos tales como líneas de pesca o anzuelos entre otros. La exposición doméstica se ve en la manipulación de peceras. La infección por M. marinum fue una vez llamada granuloma de las piscinas, aunque se ha dejado de ver después de ese tipo de exposición debido a la cloración de las piscinas. Las piscinas cloradas no se consideran exposición de riesgo.

Infección reciente de mano y antebrazo por M. marinum.
M. marinum crece mejor a 32ºC, por lo tanto, las extremidades, que son zonas frias, como las manos son áreas más afectadas respecto de las áreas centrales. Este hallazgo es también importante para el crecimiento óptimo en los laboratorios de microbiología. M. marinum puede diseminarse en individuos severamente comprometidos como los transplantados.
Frecuencia.
La frecuencia estimada es aproximadamente 0,27 casos por 100000 habitantes/año.
Manifestaciones Clínicas.
La infección por M. marinum sigue a menudo a abrasiones de una extremidad que ocurre en contacto a aguas no cloradas en pescadores deportivos o pescadores de ostras, bañistas, y trabajadores de acuarios. Tiene un período de incubación de 2 a 3 semanas.
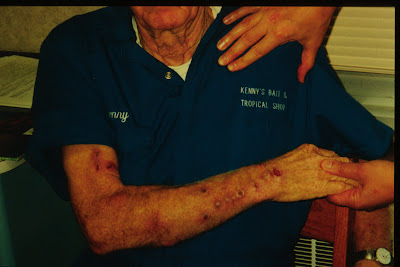
"Granuloma de las piscinas" en un paciente con infección por M. marinum de piel en región de antebrazo.
Una pápula levemente dolorosa o un nódulo aparecen en el sitio del trauma, que va creciendo lentamente para después supurar o ulcerarse. (Figuras)
La lesión crece lentamente en forma local en un período de meses. Es frecuente el dolor local y la induración. Puede haber linfangitis ascendente, pero las adenopatías reginales no son comunes. Esta linfangitis ascendente es común a otras etiologías infecciosas como esporotricosis, leishmaniasis cutánea, nocardiosis, forma úlceroglandular de la tularemia, infección por otras micobacterias no tuberculosas (Mycobacterium chelonae, Mycobacterium fortuitum, Mycobacterium kansasii), varias infecciones fúngicas como blastomicosis, histoplasmosis, criptococosis, y coccidioidomicosis, y varias bacterias piógenas (Staphylococcus aureus, Streptococcus pyogenes, Burkholderia pseudomallei, Bacillus anthracis) La diseminación a estructuras profundas (tendones, articulaciones, o aún huesos, ocurren en un tercio de los pacientes.
La lesión crece lentamente en forma local en un período de meses. Es frecuente el dolor local y la induración. Puede haber linfangitis ascendente, pero las adenopatías reginales no son comunes. Esta linfangitis ascendente es común a otras etiologías infecciosas como esporotricosis, leishmaniasis cutánea, nocardiosis, forma úlceroglandular de la tularemia, infección por otras micobacterias no tuberculosas (Mycobacterium chelonae, Mycobacterium fortuitum, Mycobacterium kansasii), varias infecciones fúngicas como blastomicosis, histoplasmosis, criptococosis, y coccidioidomicosis, y varias bacterias piógenas (Staphylococcus aureus, Streptococcus pyogenes, Burkholderia pseudomallei, Bacillus anthracis) La diseminación a estructuras profundas (tendones, articulaciones, o aún huesos, ocurren en un tercio de los pacientes.
Nódulos subcutáneos en antebrazo y dorso de manos en una paciente con einfección por M. marinum adquirida en forma ocupacional (la paciente limpiaba peceras)
La extremidad superior, principalmente las manos es la zona más afectada (90%). El compromiso profundo, con tenosinovitis, artritis séptica, osteomielitis pueden ser evidentes en el examen. La PPD es positiva de 5 a 9 mm en la mayoría de los pacientes.
Puede presentarse como un granuloma anular intersticial.
Puede presentarse como un granuloma anular intersticial.
Diagnóstico.
M. marinum crece en 2 a 3 semanas en un medio de Lowenstein-Jensen a 30ºC, por lo que hay que avisar de la sospecha al personal de laboratorio, ya que otros bacilos ácido alcohol resistentes crecen a temperaturas mayores.
M. marinum es un fotocromógeno (grupo 1 de Runyon) y produce un pigmento amarillo cuando se lo expone a la luz. Produce ureasa y catalasa débilmente pero no produce niacina ni nitrato.
Las técnicas de amplificación por PCR usando primers específicos del género Mycobacterium pueden usarse para el diagnóstico en una muestra de biopsia.
Imágenes.
La Rx puede evidenciar una osteomielitis. Una TAC o RMN si hay tenosinovitis o zonas más profundas afectadas.
Procedimientos.
El drenaje quirúrgico de las lesiones de piel a menudo no es necesario, pero el compromiso de estructuras más profundas pueden requerir debridamiento quirúrgico.
Histología.
Las lesiones recientes muestran hiperqueratosis, una respuesta inflamatoria mixta, o supuración. Las lesiones más antiguas pueden presentarse como granulomas organizados.
M. marinum crece en 2 a 3 semanas en un medio de Lowenstein-Jensen a 30ºC, por lo que hay que avisar de la sospecha al personal de laboratorio, ya que otros bacilos ácido alcohol resistentes crecen a temperaturas mayores.
M. marinum es un fotocromógeno (grupo 1 de Runyon) y produce un pigmento amarillo cuando se lo expone a la luz. Produce ureasa y catalasa débilmente pero no produce niacina ni nitrato.
Las técnicas de amplificación por PCR usando primers específicos del género Mycobacterium pueden usarse para el diagnóstico en una muestra de biopsia.
Imágenes.
La Rx puede evidenciar una osteomielitis. Una TAC o RMN si hay tenosinovitis o zonas más profundas afectadas.
Procedimientos.
El drenaje quirúrgico de las lesiones de piel a menudo no es necesario, pero el compromiso de estructuras más profundas pueden requerir debridamiento quirúrgico.
Histología.
Las lesiones recientes muestran hiperqueratosis, una respuesta inflamatoria mixta, o supuración. Las lesiones más antiguas pueden presentarse como granulomas organizados.
Tratamiento.
La piedra angular del tratamiento en la infección de M. marinum es la terapia antimicrobiana. La duración del tratamiento no está muy bien definido, pero las infecciones de piel y partes blandas debe continuarse 1 a 2 meses una vez resuelto el cuadro y las lesiones. Por lo tanto el tratamiento dura 3 a 4 meses, y más todavía cuando hay estructuras profundas comprometidas. Algunos autores han sugerido 6 meses y en algunos casos hasta 2 años. Se prefier la combinación de 2 agentes en vez de la monoterapia.
M. marinum es resistente a los tuberculostáticos isoniacida, pirazinamida y PAS, y muestra sensibilidad intermedia a la estreptomicina. El M.marinum es sensible a rifampicina, rifabutina, claritromicina, etambutol, y sulfamidas incluyendo TMS-SMX, y fluoroquinolonas. No se hacen tests de sensibilidad habitualmente y solo se reservan para los fracasos terapéuticos. La combinación de claritromicina y etambutol es la de mejor eficacia y tolerabilidad, y cuando hay osteomielitis u otras estructuras profundas están afectadas se agrega rifampicina.
El pronóstico en general es bueno con tasas de 87% de curación.
Bibliografía.
UpToDate.
The New England Journal of Medicine.
Emedicine.
Medscape.

3 comentarios:
Excelente!!!!!!!!!!!!!
It is very helpful!
MUCHAS GRACIAS QUE BUENA INFORMACIÓN!!
Publicar un comentario